题目内容
14. 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系,根据图示转化关系推测下列说法不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系,根据图示转化关系推测下列说法不正确的是( )| A. | 可用KI-淀粉试纸和食醋检验加碘盐中是否含有碘 | |
| B. | 足量Cl2能使湿润的KI-淀粉试纸变白的原因可能是:5Cl2+I2+6H2O═2HIO3+10HCl | |
| C. | 由图可知氧化性的强弱顺序为Cl2>I2>IO${\;}_{3}^{-}$ | |
| D. | 途径Ⅱ中若生成1 mol I2,反应中转移的电子数为5NA |
分析 A.加碘盐中含有NaIO3,其在酸性条件下可被I-还原生成I2;
B.根据图示转化Ⅲ可知Cl2>NaIO3,氯气可以将碘氧化HIO3;
C.由途径I可知氧化性Cl2>I2,由途径Ⅱ可知氧化性I2<NaIO3,由途径Ⅲ可知氧化性Cl2>NaIO3;
D.根据转化关系2IO3-~I2~10e-计算判断.
解答 解:A.加碘盐中含有NaIO3,其在酸性条件下可被I-还原生成I2,故用淀粉-KI试纸和食醋检验加碘盐,故A正确;
B.根据图示转化Ⅲ可知Cl2>NaIO3,已变蓝的淀粉-KI试纸褪色的原因可能是氯气将碘氧化为HIO3,反应方程式为5Cl2+I2+6H2O═2HClO3+10HCl,故B正确;
C.由途径I可知氧化性Cl2>I2,由途径Ⅱ可知氧化性I2<NaIO3,由途径Ⅲ可知氧化性Cl2>NaIO3,故氧化性的强弱顺序为Cl2>IO3->I2,故C错误;
D.根据转化关系2IO3-~I2~10e-可知,生成1 molI2反应中转移的电子数为10NA,故D错误;
故选CD.
点评 本题综合考查卤素单质及其化合物的性质,侧重于考查氧化性强弱比较及应用,难度中等,根据转化关系判断氧化性强弱是解题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.NA表示阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 12g 金刚石中含有的六元碳环数为NA | |
| B. | 1L1mol/L 的甲醇水溶液中含有氢原子总数为4NA | |
| C. | 12g 石墨和 C60的混合物中质子总数为6NA | |
| D. | 反应 KIO3+6HI=KI+3H2O+3I2中,生成1molI2转移电子的总数为2NA |
5.短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液.下列说法正确的是( )
| A. | 元素Y的最高正化合价为+6 | B. | 离子半径的大小顺序为W>Q>Z>X>Y | ||
| C. | 工业上用电解法冶炼Z单质 | D. | 元素Q的含氧酸的酸性一定比W的强 |
9.合成具有美白作用的化妆品原料Z的反应原理如下:
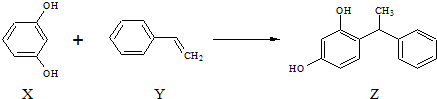
下列叙述不正确的是( )

下列叙述不正确的是( )
| A. | X、Z均能与Na2CO3溶液反应 | |
| B. | X可作缩聚反应单体,Y可作加聚反应单体 | |
| C. | X、Y、Z 均能使溴水褪色,但是原理不完全相同 | |
| D. | 该反应的反应类型为取代反应 |
19.下列有机物中,既能发生加成反应、酯化反应,又能发生氧化反应的是( )
①CH2OH(CHOH)4CHO
②CH3CH2CH2OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
①CH2OH(CHOH)4CHO
②CH3CH2CH2OH
③CH2═CH-CH2OH
④CH2═CH-COOCH3
⑤CH2═CH-COOH.
| A. | ③⑤ | B. | ②④ | C. | ①③⑤ | D. | ①③ |
6.下列物质均属于纯净物的一组是( )
| A. | 冰水混合物、TNT、溴苯、胆矾 | |
| B. | 爆鸣气、铝热剂、普通玻璃、漂白粉 | |
| C. | 二甲苯、C5H10、花生油、福尔马林 | |
| D. | 水玻璃、密封保存的NO2气体、甲醛、氯化银 |
3.下列说法正确的是( )
| A. | 乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别 | |
| B. | 乙醇和乙酸中都存在碳氧双键 | |
| C. | 常温下,Imol乙醇可与足量的金属钠反应生成11.2L氢气 | |
| D. | 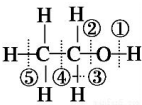 己知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③ |