题目内容
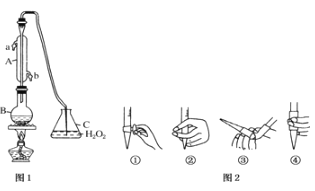
【题目】某研究性学习小组用如图装置![]() 铁架台等仪器略
铁架台等仪器略![]() 探究氧化铁与乙醇的反应,并检验反应产物。
探究氧化铁与乙醇的反应,并检验反应产物。
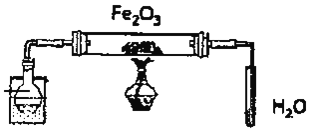
已知:![]() 乙醇的氧化产物是乙醛;
乙醇的氧化产物是乙醛;
![]() 乙醇和乙醛都易溶于水,乙醇沸点是75℃ ,是20.8℃
乙醇和乙醛都易溶于水,乙醇沸点是75℃ ,是20.8℃
(1)组装好仪器后须进行的操作是______,其方法是______
(2)圆底烧瓶中试剂的结构简式是______。
(3)本实验装置有一处不合理,如不加以改进可能会发生______。
(4)经上述实验,观察至红色的Fe2O3全部变为黑色固体。停止加热,冷却后取出硬质玻璃管中的黑色固体少许许于试管中,再加入足量稀硫酸,振荡,固体全部溶解,得到澄清溶液,实验过程中未观察到气泡产生。澄清溶液中一定含有的金属阳离子是______检验该离子的实验是______
(5)黑色固体成分用FeOx示。用下列装置测量X值。
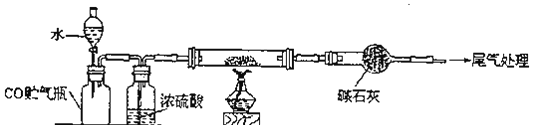
![]() 充分反应后,停止实验的操作是_______
充分反应后,停止实验的操作是_______
![]() 实验中测得数据如下
实验中测得数据如下![]() 进行的反应己完全
进行的反应己完全![]() :
:
空硬质玻璃管的质量56.0g
硬质玻璃管和FeOx的总质量79.2g
硬质玻璃管和Fe粉的总质量72.8g(冷却到室温称量![]()
反应前干燥管及内盛物的总质量48.0g
反应后干燥管及内盛物的总质量65.6g
据上述数据计算出X=______
【答案】检查装置气密性 将导管末端伸入水中,微热烧瓶,导管末端有气泡产生,停止加热,导管末端有一段稳定的水柱,说明气密性良好 CH3CH2OH 倒吸 Fe2+ 取少量澄清溶液于试管中,滴入几滴铁氰酸钾溶液,若出现蓝色沉淀证明含亚铁离子 先停止加热,等装置冷却后,再关闭分液漏斗旋塞 ![]()
【解析】
(1)气体发生的反应是需要装置气密性检验,装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;
(2)圆底烧瓶中试剂是乙醇;
(3)导气管直接插入水中可能会发生倒吸;
(4)经上述实验,观察至红色的Fe2O3全部变为黑色固体,停止加热,冷却后取出硬质玻璃管中的黑色固体少许于试管中,再加入足量稀硫酸,振荡,固体全部溶解,得到澄清溶液,实验过程中未观察到气泡产生说明无铁单质,则澄清溶液中一定含有的金属阳离子是为亚铁离子,检验亚铁离子的试剂是铁氰化钾检验;
(5)实验过程依据反应原理和实验目的分析实验步骤为,组装装置,检验装置气密性,加入试剂,加入水把一氧化碳赶入后续装置,点燃酒精灯加热玻璃管,反应结束后停止加热,关闭分液漏斗活塞,玻璃管称量剩余固体,依据质量变化计算铁元素和氧元素物质的量之比。
(1)依据装置图分析可知反应过程需要在气密性好的装置中进行,定量测定,所以气体通过装置,实验前需要检验装置气密性,依据装置图分析可知反应过程需要在气密性好的装置中进行,定量测定,所以气体通过装置,实验前需要检验装置气密性,方法为:将导管末端伸入水中,微热烧瓶,导管末端有气泡产生,停止加热,导管末端有一段稳定的水柱,说明气密性良好,
故答案为:检查装置气密性;将导管末端伸入水中,微热烧瓶,导管末端有气泡产生,停止加热,导管末端有一段稳定的水柱,说明气密性良好;
(2)圆底烧瓶中试剂的结构简式是:CH3CH2OH,
故答案为:CH3CH2OH;
(3)本实验装置有一处不合理,如不加以改进可能会发生倒吸,
故答案为:倒吸;
(4)经上述实验,观察至红色的Fe2O3全部变为黑色固体,停止加热,冷却后取出硬质玻璃管中的黑色固体少许于试管中,再加入足量稀硫酸,振荡,固体全部溶解,得到澄清溶液,实验过程中未观察到气泡产生说明无铁单质,则澄清溶液中一定含有的金属阳离子是为亚铁离子,检验亚铁离子的试剂是铁氰化钾检验,方法为:取少量澄清溶液于试管中,滴入几滴铁氰酸钾溶液,若出现蓝色沉淀证明含亚铁离子,
故答案为:Fe2+;取少量澄清溶液于试管中,滴入几滴铁氰酸钾溶液,若出现蓝色沉淀证明含亚铁离子;
(5)①充分反应后,停止实验的操作是:先停止加热,等装置冷却后,再关闭分液漏斗旋塞,
故答案为:先停止加热,等装置冷却后,再关闭分液漏斗旋塞;
②空硬质玻璃管的质量56.0g
硬质玻璃管和FeOx的总质量79.2g
,FeOx质量=79.2g-56.0g=23.2g,
硬质玻璃管和Fe粉的总质量72.8g(冷却到室温称量![]() ,生成Fe的质量=72.8g-56.0g=16.8g,物质的量
,生成Fe的质量=72.8g-56.0g=16.8g,物质的量![]() ,
,
反应前干燥管及内盛物的总质量48.0g,反应后干燥管及内盛物的总质量65.6g,为生成二氧化碳气体的质量=65.6g-48.0g=17.6g,二氧化碳物质的量![]() ,
,
所含O元素物质的量![]() ,则FeOx中
,则FeOx中![]() ,
,![]() ,
,
故答案为:![]() 。
。

【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向蛋白质溶液中加入醋酸铅溶液,产生白色沉淀 | 蛋白质发生了盐析 |
B | SO2通入Ba(NO3)2溶液中,产生白色沉淀 | 沉淀为BaSO3 |
C | 向蔗糖中加入适量浓硫酸并搅拌,蔗糖变黑,体积膨胀,并放出刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
D | 分别向等物质的量浓度的苯酚钠溶液和碳酸钠溶液中滴加酚酞,后者红色更深 | 碳酸酸性强于苯酚 |
A.AB.BC.CD.D
【题目】草酸(H2C2O4)是一种重要的有机化工原料,为探究草酸的制取和草酸的性质,进行如下实验:
实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如图所示:
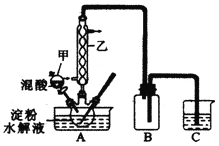
①一定量的淀粉水解液加入三劲烧瓶中
②控制反应温度55~60℃,边搅拌边缓慢滴加一定量的混合酸(65%的H2SO4与98%的H2SO4的质量比为2:1.25)
③反应3小时,冷却,有随后再重结晶得到草酸晶体硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
(1)装置B的作用是 ______
(2)如何检验该装置的气密性: ______
(3)要控制反应温度55~60℃,应选择加热的方式是 ______,C装置中应加入 ______溶液。
实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:______
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快,为探究其原因,同学们做了如下对比实验:
实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(s) 质量(g) | 褪色时间(g) | ||
c(mol/L) | V(mL) | c(mol/L) | V(mL) | |||
实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
由此你认为溶液褪色总是先慢后快的原因是 ______
(6)为测定上述实验中得到草酸的纯度,取5.0 g该草酸样品,配制成250 mL溶液,然后取25.00 mL此溶液溶于锥形瓶中,将0.10 mol/L酸性KMnO4溶液装在 ______(填仪器名称)中进行滴定,达到滴定终点时的现象是 ______,若消耗酸性KMnO4溶液体积为20.00 mL,则该草酸样品的纯度为 ______。
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量,某兴趣小组进行下面实验探究,查阅资料知道:
①2NO + Na2O2=2NaNO2
②2NO2+ Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-还原成Mn2+。
Ⅰ.产品制备与检验:用如下装置制备NaNO2:

(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目________。
(2)B装置的作用是______________________________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净NaNO2应在B、C装置间增加一个装置,请在框内画出增加的装置图,并标明盛放的试剂________。

(4)试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论)________。
Ⅱ.含量的测定
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
(5)第一组实验数据出现异常,造成这种异常的原因可能是________(双项选择)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
D.滴定终了俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数____________________。
(结果保留4位有效数字)