题目内容
4.据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为2Zn+O2═2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是( )| A. | 锌为正,空气进入负极反应 | B. | 负极反应为Zn+2OH--2e-═ZnO+H2O | ||
| C. | 正极发生氧化反应 | D. | 电解液可以是强酸也可以是强碱 |
分析 根据化合价变化可知Zn被氧化,作原电池的负极,负极上锌失电子发生氧化反应,正极上氧气得电子发生还原反应,以此解答该题.
解答 解:A.锌失去电子化合价升高,发生氧化反应作原电池负极,氧气得到电子发生还原反应,所以空气进入正极进行反应,故A错误;
B.锌作负极,负极上锌失电子得到ZnO,负极反应为:Zn+2OH--2e-═ZnO+H2O,故B正确;
C.正极上得电子发生还原反应,故C错误;
D.氧化锌能溶于酸,所以电解质溶液一定不是强酸,故D错误.
故选B.
点评 本题考查了原电池知识,题目难度不大,注意根据电池反应判断原电池的正负极以及电极反应.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
19.常温下将一定浓度的某一元酸HA和0.1mol/L NaOH溶液等体积混合后,下列说法正确的是( )
| A. | 若pH=7,c(HA)=0.1 mol/L | |
| B. | 若pH<7,微粒浓度关系可能为:c(Na+)=c(HA)+c(A-) | |
| C. | 若pH>7,c(A-)>c(Na+) | |
| D. | 若pH=12,且HA为强酸时,c(HA)=0.08 mol/L |
9.为了除去CO2中的O2、SO2、H2O(g)等杂质,可用①NaHCO3饱和溶液②浓硫酸③加热的铜网,通过以上试剂顺序净化效果最好的是( )
| A. | ②③① | B. | ③② | C. | ②①③ | D. | ①②③ |
16.下面关于电解质的叙述中正确的是( )
| A. | 在水溶液中或熔融状态下均不导电的化合物叫非电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | 电解质在水中一定能导电,在水中导电的化合物一定是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
13.下列在溶液中能大量共存的离子组是( )
| A. | K+,H+,SO42-,S2- | B. | Na+,Ca2+,NO3-,SO42- | ||
| C. | Cu 2+,Mg2+,Cl-,S2- | D. | Na+,Cu2+,Cl-,SO42- |
14.下列关于氧化还原反应的叙述中正确的是( )
| A. | 失去电子的反应为还原反应 | B. | 含有氧元素的物质是氧化剂 | ||
| C. | 还原剂是化合价升高的物质 | D. | 氧化剂和还原剂不可能是同一物质 |
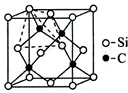 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.回答下列问题:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.回答下列问题: