题目内容
同温同压下,同体积的NH3和H2S气体的质量比是 ;同质量的NH3和H2S气体的体积比是 ;同质量的NH3和H2S气体中所含氢原子个数比是 ;若两者所含氢原子个数相等,它们的物质的量比是 .
考点:阿伏加德罗定律及推论
专题:
分析:同温同压下,气体摩尔体积相等,根据m=
M计算其质量之比,根据V=
Vm计算其体积之比,根据N=
NA结合分子构成计算H原子个数之比,根据H原子个数及分子构成计算其物质的量之比.
| V |
| Vm |
| m |
| M |
| m |
| M |
解答:
解:同温同压下,气体摩尔体积相等,根据m=
M知,相同体积的NH3和H2S气体的质量比为其摩尔质量之比=17g/mol:34g/mol=1:2,根据V=
Vm知,同质量的NH3和H2S气体的体积比为其摩尔质量之比的反比=34g/mol:17g/mol=2:1,
根据N=
NA知,其分子数之比等于其摩尔质量的反比=34g/mol:17g/mol=2:1,结合分子构成知,其H原子个数之比为3:1,若两者所含氢原子个数相等,根据分子构成知,其分子个数之比为2:3,根据N=nNA知,其物质的量之比为2:3,
故答案为:1:2;2:1;3:1;2:3.
| V |
| Vm |
| m |
| M |
根据N=
| m |
| M |
故答案为:1:2;2:1;3:1;2:3.
点评:本题考查了阿伏伽德罗定律及其推论,明确各个物理量之间的关系是解本题关键,根据基本公式来分析解答即可,题目难度不大.

练习册系列答案
相关题目
X、Y是元素周期表ⅦA族中的两种元素.下列叙述中能说明X的非金属性比Y强的是( )
| A、Y离子的还原性比X离子的还原性弱 |
| B、Y的最高价含氧酸的酸性比X的最高价含氧酸的酸性弱 |
| C、Y的气态氢化物比X的气态氢化物稳定 |
| D、Y的单质能将X从NaX的溶液中置换出来 |
下列电离方程式中,不正确的是( )
| A、NaCl═Na++Cl- |
| B、CH3COOH?CH3COO-+H+ |
| C、NH3?H2O═NH4++OH- |
| D、NaOH═Na++OH- |
下列说法正确的是( )
| A、炒过菜的铁锅不及时清洗易生锈 |
| B、铁发生电化学腐蚀时铁为正极 |
| C、轮船吃水线以下的船壳外焊上锌块,可以防止铁船体被腐蚀 |
| D、经常用钢丝球擦洗铝锅表面,可以防止铝锅被腐蚀 |
根据图,下列判断中正确的是( )


| A、烧杯a中的溶液pH不变 |
| B、烧杯a中发生氧化反应 |
| C、烧杯a中发生的反应为2H2O+2e-═H2↑+2OH- |
| D、烧杯b中发生的反应为Zn-2e-═Zn2+ |
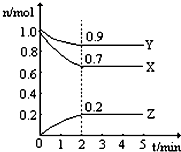 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线,如图所示.根据图中数据,试填写下列空白: 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.