题目内容
15.在体积均为1L,pH均为2的盐酸和醋酸溶液中,分别投入0.23gNa,下列示意图中正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 pH均等于2的盐酸和醋酸溶液,开始氢离子浓度相同,pH相同,但醋酸为弱酸,则醋酸的浓度大于盐酸的浓度,与等量的Na反应时,醋酸生反应速率大,以此来解答.
解答 解:A.醋酸与Na反应生成的醋酸钠溶液中,因醋酸根离子水解显碱性,但醋酸过量,溶液显酸性,所以溶液的pH<7,故A错误;
B.因盐酸与Na恰好完全反应,则反应后溶液的pH=7,而醋酸过量,溶液显酸性,所以溶液的pH<7,故B正确;
C.因Na的质量相同,则与盐酸恰好完全反应,醋酸过量,生成氢气相同,故C错误;
D.因Na的质量相同,则与盐酸恰好完全反应,醋酸过量,生成氢气相同,且醋酸中氢离子浓度大于盐酸中氢离子浓度,则醋酸先反应结束,故D错误;
故选B.
点评 本题考查酸与金属的反应及图象分析,明确酸的强弱、pH与浓度的关系、图象中纵横坐标的含义是解答本题的关键,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
18.下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的元素是Mg(填“元素符号”),金属性最强的元素是F(填“元素符号”),化学性质最不活泼的元素是Ar(填“元素符号”).
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
3.下列化学用语中,书写或说法正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 丙烷的球棍模型为 | |
| C. | 乙醇含有的官能团是-OH,带一个单位负电荷 | |
| D. | 乙酸的分子式为C2H4O2,其中CH3-在溶液中能电离出H+ |
20.取pH=2的盐酸和醋酸各100毫升,再分别加入0.65克锌粉,在相同条件下充分反应后,有关叙述正确的是( )
| A. | 刚开始醋酸与锌反应速率大 | |
| B. | 反应过程中盐酸和醋酸分别与锌反应的速率一样大 | |
| C. | 醋酸与锌反应放出的氢气多 | |
| D. | 锌分别与醋酸、盐酸反应产生的氢气一样多 |
7. 如表是元素周期表中短周期部分,表中所列字母分别代表一种元素.
如表是元素周期表中短周期部分,表中所列字母分别代表一种元素.
根据上述元素回答问题:(本题用化学用语回答)
(1)上述元素中地壳中极为丰富的元素O,单质中熔点最高的可能是C,E、F、G离子半径由小到大的顺序是Na+<F-<Cl-,写出化合物A2D2的电子式 ;
;
(2)A、B、D、F四种元素组成的受热易分解的化合物,写出少量该化合物溶液与足量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(3)化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),图中表示反应速率与反应过程的关系,其中表示平衡混合物中CA3含量最高的一段时间是t0~t1.温度为T℃时,将4mol A2和2mol C2放入1L密闭容器中,60s后测得C2的转化率为50%,则A2的反应速率为0.05mol/(L﹒s).
 如表是元素周期表中短周期部分,表中所列字母分别代表一种元素.
如表是元素周期表中短周期部分,表中所列字母分别代表一种元素.| A | |||||||
| B | C | D | E | ||||
| F | G | H | |||||
(1)上述元素中地壳中极为丰富的元素O,单质中熔点最高的可能是C,E、F、G离子半径由小到大的顺序是Na+<F-<Cl-,写出化合物A2D2的电子式
 ;
;(2)A、B、D、F四种元素组成的受热易分解的化合物,写出少量该化合物溶液与足量Ba(OH)2溶液反应的离子方程式Ba2++HCO3-+OH-═BaCO3↓+H2O.
(3)化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),图中表示反应速率与反应过程的关系,其中表示平衡混合物中CA3含量最高的一段时间是t0~t1.温度为T℃时,将4mol A2和2mol C2放入1L密闭容器中,60s后测得C2的转化率为50%,则A2的反应速率为0.05mol/(L﹒s).
4.下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)画出元素④的原子结构示意图 ,⑦元素的名称是硅,⑨元素的离子的电子式是
,⑦元素的名称是硅,⑨元素的离子的电子式是 ,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
(2)在标号元素中,最活泼的金属元素是(写元素符号)Na.最活泼的非金属元素是(写元素符号)F.
(3)⑦、⑧、⑨元素所形成的气态氢化物中,最稳定的是(写化学式)HCl.
(4)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是(写元素符号)Na>Al>Si.
(5)①与③形成共价化合物的电子式 .用电子式表示⑤与⑧形成化合物的形成过程
.用电子式表示⑤与⑧形成化合物的形成过程 .
.
(6)⑦、⑧、⑨三种元素的最高价含氧酸的酸性由强到弱的顺序是(写化学式)HClO4>H2SO4>H2SiO3.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 ,⑦元素的名称是硅,⑨元素的离子的电子式是
,⑦元素的名称是硅,⑨元素的离子的电子式是 ,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).
,②的最简单气态氢化物中的化学键有极性键(填“离子键”、“极性键”或“非极性键”).(2)在标号元素中,最活泼的金属元素是(写元素符号)Na.最活泼的非金属元素是(写元素符号)F.
(3)⑦、⑧、⑨元素所形成的气态氢化物中,最稳定的是(写化学式)HCl.
(4)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是(写元素符号)Na>Al>Si.
(5)①与③形成共价化合物的电子式
 .用电子式表示⑤与⑧形成化合物的形成过程
.用电子式表示⑤与⑧形成化合物的形成过程 .
.(6)⑦、⑧、⑨三种元素的最高价含氧酸的酸性由强到弱的顺序是(写化学式)HClO4>H2SO4>H2SiO3.
 ;
; (写结构简式),它的一氯代物有1种.
(写结构简式),它的一氯代物有1种. ;
; ;
; +2Ag+3NH3+H2O;
+2Ag+3NH3+H2O; .
. (不考虑立体结构).M的新旧二条合成路线如下:
(不考虑立体结构).M的新旧二条合成路线如下:



 D
D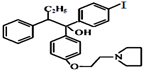
 有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有多少种.6任写其中一种的结构简式.
有多种同分异构体,其中满足①遇FeCl3显色②苯环上的一溴取代物只有一种,符合条件的同分异构体数目有多少种.6任写其中一种的结构简式. 中任一种
中任一种 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +HBr
+HBr 及含二个碳原子的有机化合物为原料,制备芳香醇
及含二个碳原子的有机化合物为原料,制备芳香醇 的合成路线(不超过5步反应).
的合成路线(不超过5步反应).