题目内容
【题目】用铝箔包装0.1mol金属钠,用针扎一些小孔,放入水中,完全反应后,用排水取气法收集产生的气体,则收集到气体的为 ( )
A. O2和H2的混合气体 B. 0.05molH2
C. 小于0.05molH2气体 D. 大于0.05molH2
【答案】D
【解析】根据2Na+2H2O=2NaOH+H2↑知,0.1molNa和水反应生成氢气的物质的量为0.05mol,根据2Al+2NaOH+2H2O=2NaAlO2+3H2↑知,NaOH和Al反应生成氢气,所以最终得到氢气的物质的量大于0.05mol,故选D。

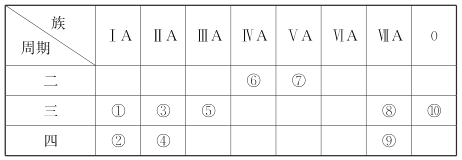
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,回答下列问题:
主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)元素①的名称是_____________;比元素⑧质子数多10的元素在周期表中所处位置___________。
(2)元素③的单质的电子式为_____________,元素③的气态氢化物与其最高价氧化物的水化物反应的化学方程式为_________________________________________。
(3)用电子式表示元素⑨与⑥的化合物的形成过程:____________________________,该化合物属于__________(填“共价或“离子”)化合物。
(4)表示②与⑦形成的化合物的电子式:________________________,该化合物是由__________(填“极性”或“非极性”)键形成的。
(5)元素⑥的氢化物的结构式为_____________________;该氢化物常温下和元素⑦的单质反应的化学方程式为________________________________;元素③④⑥形成的氢化物沸点由高到底的顺序(写化学式)___________________________。
(6)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)__________________________________。
(7)某原子有6个电子、7个中子,写出其元素符号:________________________。
(8)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为:4核18电子的分子_____________________,10电子的阳离子_______________________________。