题目内容
下列实验能成功的是( )
| A、直接蒸馏法分离乙酸和乙醇混合液 |
| B、苯和浓溴水在Fe作催化剂条件下反应制溴苯 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴葡萄糖溶液,加热 |
考点:化学实验方案的评价,苯的性质,溴乙烷的化学性质,葡萄糖的性质和用途
专题:实验评价题
分析:A.利用蒸馏法分离乙醇和乙酸需要控制温度;
B.在铁作催化剂条件下,苯和液溴发生取代反应制取溴苯;
C.溴乙烷中没有自由移动的溴离子,和硝酸银溶液不反应;
D.在加热、碱性条件下,葡萄糖和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀.
B.在铁作催化剂条件下,苯和液溴发生取代反应制取溴苯;
C.溴乙烷中没有自由移动的溴离子,和硝酸银溶液不反应;
D.在加热、碱性条件下,葡萄糖和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀.
解答:
解:A.乙醇和乙酸的沸点不同,利用蒸馏法分离乙醇和乙酸需要控制温度,故A错误;
B.在铁作催化剂条件下,苯和液溴发生取代反应制取溴苯,苯和溴水不反应,故B错误;
C.溴乙烷中没有自由移动的溴离子,和硝酸银溶液不反应,要检验溴元素,需要将溴乙烷和氢氧化钠的水溶液发生取代反应生成溴离子,再利用硝酸银溶液检验溴离子,故C错误;
D.在加热、碱性条件下,葡萄糖和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀氧化亚铜,该实验能检验醛基,故D正确;
故选D.
B.在铁作催化剂条件下,苯和液溴发生取代反应制取溴苯,苯和溴水不反应,故B错误;
C.溴乙烷中没有自由移动的溴离子,和硝酸银溶液不反应,要检验溴元素,需要将溴乙烷和氢氧化钠的水溶液发生取代反应生成溴离子,再利用硝酸银溶液检验溴离子,故C错误;
D.在加热、碱性条件下,葡萄糖和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀氧化亚铜,该实验能检验醛基,故D正确;
故选D.
点评:本题考查了物质的分离和提纯、元素或官能团的检验等知识点,利用沸点不同采用蒸馏的方法分离互溶的液体,知道卤代烃中卤元素的检验方法,在加入硝酸银溶液前要加入酸中和未反应的碱,否则会导致实验失败,为易错点.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
标准状况下,电解一定物质的量浓度的CuSO4溶液一段时间后,加入0.1mol Cu(OH)2固体使溶液完全恢复到初始状态,则此过程中共产生气体( )
| A、6.72L | B、8.96L |
| C、4.48L | D、5.6L |
烷烃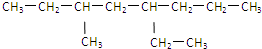 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
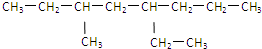 是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )
是由含有一个三键的炔烃与氢气加成后的产物,此炔烃可能的结构有( )| A、1种 | B、2种 | C、3种 | D、4种 |
在温度不变、恒容的容器中进行反应A2?2A△H>0,若反应物浓度由0.1mol?L-1降到0.06mol?L-1需20s,那么由0.06mol?L-1降到0.02mol?L-1,所需反应时间应( )
| A、等于20s | B、小于20s |
| C、大于20s | D、无法确定 |
下列化合物分子中既有离子键又有共价键的是( )
| A、BaCl2 |
| B、Na2O |
| C、(NH4)2SO4 |
| D、H2SO4 |
往下列溶液中,通入足量CO2气体,最终能析出固体的是( )
| A、澄清石灰水 |
| B、饱和Na2CO3溶液 |
| C、CaCl2溶液 |
| D、盐酸 |
下列反应的能量变化属于吸热反应的是( )
| A、氯化铵与Ba(OH)2?8H2O的反应 |
| B、氢氧化钠溶液与盐酸反应 |
| C、锌片与稀硫酸反应 |
| D、钠与冷水反应 |
工业上用H2和N2直接合成氨:N2+3H2═2NH3,下列措施肯定能使合成氨反应速率加快的是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强.
| A、只有①②③ | B、只有①②④ |
| C、只有①③④ | D、①②③④ |