题目内容
9.在密闭容器中充入一定量的N2 和H2,在一定条件下发生反应:N2+3H2?2NH3.下列说法错误的是( )| A. | 使用合适催化剂可以加快反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 达到化学平衡时,N2、H2和NH3物质的量浓度一定相等 | |
| D. | 若反应在密闭容器中进行,N2和H2不可能100%转化为NH3 |
分析 A、使用催化剂加快化学反应速率;
B、温度越高反应速率越快;
C、到平衡后物质浓度不变,依据起始量和转化率分析,平衡浓度不一定相同;
D、达反应是可逆反应不能进行彻底.
解答 解:A、使用催化剂加快化学反应速率,所以使用合适催化剂化学反应速率加快,故A正确;
B、温度越高反应速率越快,故B正确;
C、达到平衡后物质浓度不变,依据起始量和转化率方向,平衡浓度不一定相同,故C错误;
D、反应是可逆反应不能进行彻底,恒温条件下达到化学平衡时,N2不能完全转化为NH3,故D正确;
故选C.
点评 本题考查了化学平衡影响因素分析判断,注意可逆反应不能进行彻底的特征,题目难度中等.

练习册系列答案
相关题目
19.下列元素中,处于元素周期表金属与非金属分界线附近的是( )
| A. | Ca | B. | Si | C. | He | D. | O |
20.以下说法正确的是( )
| A. | C70与金刚石一样属于原子晶体 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | I2升华破坏了共价键 | |
| D. | HCl溶于水能电离子出H+、Cl-,所以HCl是离子化合物 |
4.化学与人类生活、生产和社会可持续发展密切相关,下列说法正确的是( )
| A. | 为测定熔融氢氧化钠的导电性,可将氫氧化钠固体放在石英坩埚中加热熔化 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝的冶炼方法比较简单 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计箅机芯片的材料是经提纯的二氧化硅 |
1.下列操作会导致所配的溶液浓度偏高的是( )
| A. | 定容时仰视刻度线 | |
| B. | 定容后摇匀、静置,发现液面低于刻度线,又加水至刻度线 | |
| C. | 烧杯中的溶液未冷却至室温就将溶液移到容量瓶中 | |
| D. | 容量瓶洗涤后仍有少量残留 |
19.短周期的元素中,同族元素的原子序数的差值不可能是( )
| A. | 2 | B. | 8 | C. | 16 | D. | 18 |

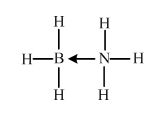 (必须标明配位犍).
(必须标明配位犍).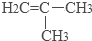 .
. .
.