题目内容
15.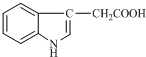 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸与苯丙氨酸互为同分异构体 | |
| B. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应 | |
| C. | 1mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5mol H2 | |
| D. | 吲哚乙酸苯环上的二氯代物共有四种结构 |
分析 有机物含有羧基,具有酸性,可发生中和、酯化反应,含有碳碳双键,可发生加成、加聚和氧化反应,结合有机物的结构解答该题.
解答 解:A.该有机物分子比苯丙氨酸多1个碳原子,分子式不同,不是同分异构体,故A错误;
B.含有碳碳双键,可发生加成、氧化和还原反应,含有羧基,可发生取代反应,故B正确;
C.苯环、碳碳双键可与氢气发生加成反应,则1mol吲哚乙酸与足量氢气发生加成反应时,可以消耗4mol H2,故C错误;
D.苯环有4个H原子可被取代,如图: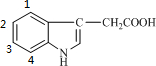 ,可取代位置有1,2;1,3;1,4;2,3,2,4;3,4,共6种结构,故D错误.
,可取代位置有1,2;1,3;1,4;2,3,2,4;3,4,共6种结构,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
相关题目
5.下列物质中均含有酸性杂质,除去这些杂质的方法中正确的是( )
| A. | 乙醇中含乙酸杂质:加入足量氧化钙,蒸馏 | |
| B. | 制氯气时,依次通过饱和NaHCO3溶液和浓硫酸净化气体 | |
| C. | CO2中混有H2S通过足量的浓硫酸溶液洗气,以得到纯净的CO2 | |
| D. | 通过灼热的镁粉除去N2中的O2 |
10. 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO
(2)同浓度的CH3COO-、HCO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大.
 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO
(2)同浓度的CH3COO-、HCO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大.
20.如表是25℃时某些弱酸的电离平衡常数.
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
(2)pH 相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是:CH3COONa>NaClO,两溶液中:[c(Na+)-c(ClO-)]=[c(K+)-c(CH3COO-)](填“>”“<”或“=”).
(3)向 0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液 pH=5.
(4)碳酸钠溶液中滴加少量氯水的离子方程式为Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO-.
| 化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(2)pH 相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是:CH3COONa>NaClO,两溶液中:[c(Na+)-c(ClO-)]=[c(K+)-c(CH3COO-)](填“>”“<”或“=”).
(3)向 0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液 pH=5.
(4)碳酸钠溶液中滴加少量氯水的离子方程式为Cl2+2CO32-+H2O═2HCO3-+Cl-+ClO-.
7.下列混合物可采用蒸馏法分离的一组是( )
| A. | 水与四氯化碳 | B. | 食盐与泥沙 | C. | 硝酸钾与氯化钾 | D. | 溴与四氯化碳 |
4.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在0℃、101 kPa时,22.4L氢气中含有NA个氢原子 | |
| B. | NA个CO分子和0.5mol CH4的质量比为7:4 | |
| C. | 16gCH4与18gNH${\;}_{4}^{+}$所含质子数相等 | |
| D. | 常温常压下,92g的NO2和N2O4混合气体中含有的原子数为6NA |
3.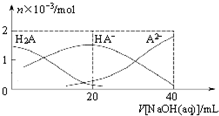 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )| A. | H2A属于强酸 | |
| B. | $\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大而减小 | |
| C. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol•L-1 | |
| D. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |