题目内容
 某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种离子,某学生小郭设计方案对废液进行如下处理,根据实验流程图,下列说法不正确的是( )
某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种离子,某学生小郭设计方案对废液进行如下处理,根据实验流程图,下列说法不正确的是( )| A、沉淀1的成分是Fe、Cu、Ag |
| B、溶液2中滴加KSCN溶液呈红色 |
| C、可排放废水中含有的阳离子主要是Na+离子 |
| D、步骤②的离子方程式是2Fe2++H2O2+2H+=2 Fe3++2 H2O |
考点:金属的回收与环境、资源保护
专题:几种重要的金属及其化合物
分析:废液中含有Fe3+、Cu2+、Ag+三种离子,加入过量铁粉后过滤,所得的沉淀1为Fe、Cu、Ag,滤液1中的阳离子为Fe2+;向滤液1中加H2O2溶液,能将Fe2+氧化为Fe3+,故滤液2中的阳离子为Fe3+;向滤液2中加强碱,能将Fe3+沉淀为Fe(OH)3,故沉淀2为Fe(OH)3;而可排放废水中含的阳离子取决于加入的强碱.
解答:
解:A、废液中含有Fe3+、Cu2+、Ag+三种离子,加入过量铁粉后,能将Cu2+、Ag+还原为Cu、Ag,能将Fe3+还原为Fe2+,故所得的沉淀1为Fe、Cu、Ag,故A正确;
B、向滤液1中加H2O2溶液,能将Fe2+氧化为Fe3+,故滤液2中的阳离子为Fe3+,故向溶液2中滴加KSCN溶液呈红色,故B正确;
C、可排放废水中含的阳离子取决于加入的强碱,如果加入的强碱不是NaOH,可排放废水中含有的阳离子则不是Na+离子,故C错误;
D、滤液1中加H2O2溶液,能将Fe2+氧化为Fe3+,离子方程式是2Fe2++H2O2+2H+=2 Fe3++2 H2O,故D正确.
故选C.
B、向滤液1中加H2O2溶液,能将Fe2+氧化为Fe3+,故滤液2中的阳离子为Fe3+,故向溶液2中滴加KSCN溶液呈红色,故B正确;
C、可排放废水中含的阳离子取决于加入的强碱,如果加入的强碱不是NaOH,可排放废水中含有的阳离子则不是Na+离子,故C错误;
D、滤液1中加H2O2溶液,能将Fe2+氧化为Fe3+,离子方程式是2Fe2++H2O2+2H+=2 Fe3++2 H2O,故D正确.
故选C.
点评:本题考查了废水的处理,应注意每步所加试剂的作用、目的和所发生的反应,难度不大,关键在流程分析.

练习册系列答案
相关题目
下列仪器中,需要垫石棉网加热的是( )
A、 |
B、 |
C、 |
D、 |
如图为某一工业合成简单理想的流程图,反应条件已省略.有关上述过程的说法错误的是( )
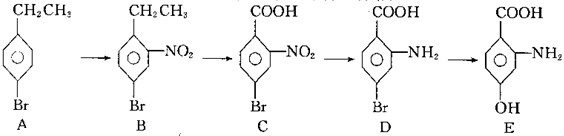

| A、物质E的化学式为C7H7NO3 |
| B、C转化为D的反应类型是还原反应 |
| C、D转化为E时,所加的反应物可以是氢氧化钠溶液和稀H2SO4 |
| D、物质A属于芳香烃 |
某烃结构如图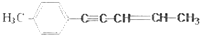 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )
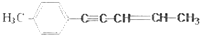 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )| A、所有原子可能在同一平面上 |
| B、在同一条直线上的碳原子最多有8个 |
| C、所有碳原子可能在同一平面上 |
| D、在同一平面上的原子最多有18个 |
下列有关合金的说法中正确的是( )
| A、构成合金的元素一定都是金属元素 |
| B、合金的熔点一般比各成分金属的熔点高 |
| C、在一般情况下,合金比纯金属的硬度小 |
| D、目前我国流通的硬币是由合金材料制造的 |
室温,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如表所示,下列说法不正确的是:( )
| 实验编号 | 起始浓度/mol/L | 反应后溶液pH | |
| c(HA) | c(KOH) | ||
| ① | 0.05 | 0.05 | 8 |
| ② | 0.1 | x | 7 |
| A、实验①中:C(K+)-C(A-)=9.9×10-7mol/L |
| B、实验②中C(K+)=C(A-)>C(H+)=C(OH-) |
| C、实验②中反应后溶液中C(K+)=0.05mol/L |
| D、若将实验②中HA换成氯水,反应后溶液pH=7,则有C(K+)=2C(ClO-)+C(HClO) |
相同温度相同物质的量浓度的三种溶液:①CH3COONa②NaHSO4③NaCl,按pH由大到小的顺序排列,正确的是( )
| A、③>②>① |
| B、①>③>② |
| C、①>②>③ |
| D、③>①>② |
一定温度下,向体积为2L的密闭容器中充入1mol PCl5(g),发生反应:PCl5(g)?PCl3(g)+Cl2(g)△H=+QKJ?mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示.下列说法正确的是( )


| A、0-3s内,容器中气体的压强不断增大 |
| B、达到平衡时放出0.6QkJ热量 |
| C、其他条件不变,升高温度,平衡常数减小 |
| D、其他条件不变,再向容器中充入1molPCl5(g),则达到平衡时,c(PCl5)>0.4mol?L-1 |
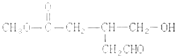
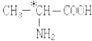 ,有机物A的结构简式如图所示:
,有机物A的结构简式如图所示: