题目内容
16.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 标准状况下,22.4L H2S全部溶于水所得溶液中HS-和S2-离子数之和为NA | |
| B. | 含4mol HCl的浓盐酸与足量二氧化锰反应转移的电子总数为2NA | |
| C. | 11g T2O含有的电子数为5NA | |
| D. | 常温下,0.2L 0.5mol/L NH4NO3溶液的氮原子数小于0.2NA |
分析 A、H2S是弱酸,在溶液中不能完全电离;
B、二氧化锰只能与浓盐酸反应,和稀盐酸不反应;
C、超重水的摩尔质量为22g/mol;
D、1mol硝酸铵中含2molN原子.
解答 解:A、H2S是弱酸,在溶液中不能完全电离,故溶液中的H2S、HS-和S2-离子数之和为NA,故A错误;
B、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故4mol盐酸不能完全反应,则转移的电子数小于2NA个,故B错误;
C、超重水的摩尔质量为22g/mol,故11g超重水的物质的量为0.5mol,则含有的电子为5NA个,故C正确;
D、1mol硝酸铵中含2molN原子,故在0.2L0.5mol/L的硝酸铵溶液中,硝酸铵的物质的量为0.1mol,则含有的N原子数为0.2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
6.将mg铜粉和镁粉的混合物分成两等份,其中一份加入100mL的稀硝酸中并加热,固体和硝酸恰好完全反应,反应前后溶液体积变化忽略不计,反应产生NO、NO2(不考虑N2O4的影响)混合气体4.48L(标准状况下);将另一份在空气中充分加热至恒重,称得固体质量增加3.2g.下列有关说法中正确的是( )
| A. | 无法确定硝酸的浓度 | B. | n(NO):n(NO2)=1:1 | ||
| C. | 4.8<m<12.8 | D. | 反应后c(NO${\;}_{3}^{-}$)=4mol/L |
4.下列表示物质结构的化学用语或模型正确的是( )
| A. | HClO的结构式:H-O-Cl | B. | HF的电子式: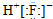 | ||
| C. | S2-的结构示意图: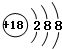 | D. | CCl4分子的比例模型: |
1.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molCl2作为反应物,转移电子数一定为2NA | |
| B. | 1molC9H20中含有共价键数目为28NA | |
| C. | 标况下448mL二氯甲烷中含有分子数为0.02NA | |
| D. | 常温常压下,1.8 g重水(D2O)中含中子数为NA |
8.下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 常温下,将Al箔插入浓HNO3中,无明显现象 | 铝和浓硝酸不反应 |
| B | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| C | 用铂丝蘸取溶液进行焰色反应,观察到火焰呈黄色 | 该溶液一定是钠盐溶液 |
| D | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| A. | A | B. | B | C. | C | D. | D |
5.对中国古代著作涉及化学的叙述,下列解说错误的是( )
| A. | 《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 | |
| B. | 《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 | |
| C. | 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 | |
| D. | 《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 |
6.如图所示,甲、乙两装置中除了铁片与铜片是否用导线连接外,其余均完全相同.若实验同时开始进行,当反应相同的时间时(反应均未停止),忽略电解质溶液的体积变化,则两装置中仍相同的是( )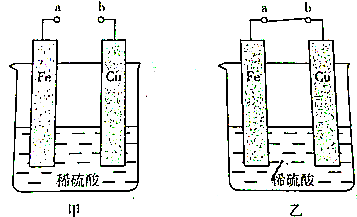

| A. | 铁片的质量 | B. | 铜片的质量 | ||
| C. | 生成氢气的体积(同温同压) | D. | H+的物质的量浓度 |
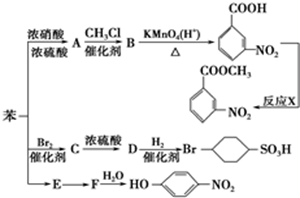
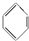 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O,其反应类型为取代反应.
+H2O,其反应类型为取代反应.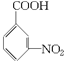 +CH3OH
+CH3OH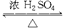
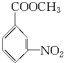 +H2O.
+H2O.