题目内容
1.下列各组中的两种物质作用,反应条件(如温度等)或反应物用量改变,不会引起产物种类改变的是( )| A. | Na和O2 | B. | NaOH和CO2 | C. | AlCl3和NaOH | D. | Na2O2和CO2 |
分析 A.钠与氧气在加热条件下生成过氧化钠,常温下生成氧化钠;
B.氢氧化钠与二氧化碳反应生成,二氧化碳少量生成碳酸钠,二氧化碳过量生成碳酸氢钠;
C.氯化铝与氢氧化钠反应,氢氧化钠少量生成氢氧化铝沉淀,氢氧化钠过量反应生成偏铝酸钠;
D.二者反应生成碳酸钠和氧气.
解答 解:A.钠与氧气在加热条件下生成过氧化钠,常温下生成氧化钠,反应产物与温度有关,故A不选;
B.氢氧化钠与二氧化碳反应生成,二氧化碳少量生成碳酸钠,二氧化碳过量生成碳酸氢钠,反应产物与二氧化碳的用量有关,故B不选;
C.氯化铝与氢氧化钠反应,氢氧化钠少量生成氢氧化铝沉淀,氢氧化钠过量反应生成偏铝酸钠,反应产物与氢氧化钠用量有关,故C不选;
D.过氧化钠与二氧化碳反应,产物与反应条件(如温度等)或反应物用量无关,故D选;
故选:D.
点评 本题考查了物质之间反应产物的判断,明确物质的性质、熟悉反应条件或反应物用量对反应的影响是解题关键,题目难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
11.两烧杯中分别盛有100mL3mol/L的硫酸溶液或100mL3mol/L的氢氧化钠溶液(先后顺序不确定),向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为3:4,下列说法正确的是( )
| A. | 参加反应的H2SO4为0.2mol | B. | 参加反应的NaOH约为0.27mol | ||
| C. | 加入铝粉的质量为5.4g | D. | 与硫酸反应的铝粉的质量7.2g |
12.下列装置中,能对Fe片腐蚀起防护作用的是( )

| A. | ③④ | B. | ②⑤ | C. | ①③④ | D. | ②③④⑤ |
9.在C4H11N中,N原子以三个单键与其他原子相连接,它具有的同分异构体的数目为( )
| A. | 6 | B. | 7 | C. | 8 | D. | 9 |
6.下列各组中的物质,互为同系物的是( )
| A. | 乙醇与丙三醇 | B. | C6H5OH与C6H5CH2OH | ||
| C. | 重氢与超重氢 | D. | 新戊烷与正丁烷 |
13.青蒿素结构式如图所示.下列有关青蒿素的说法错误的是( )
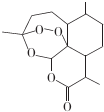

| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素分子结构稳定,受热不易分解 | |
| C. | 青蒿素可溶于NaOH溶液,可使酸性高锰酸钾溶液褪色 | |
| D. | 青蒿素难溶于水,提取的方法是用有机溶剂萃取后蒸馏 |
10.一种微生物燃料电池工作原理示意图如下,微生物膜中的酶作催化剂.下列叙述不正确的是( )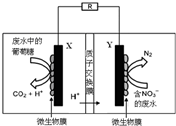

| A. | 电池工作时,既能净化废水,又能发电 | |
| B. | X电极为负极,工作时发生氧化反应 | |
| C. | 正极反应式为2NO3-+10e-+6H2O═N2↑+12OH- | |
| D. | 该电池在常温和高温时都可以工作 |
11.钢铁、铝合金、铜合金这三种合金具有广泛的用途下列说法正确的是( )
| A. | 碳钢与生铁主要成分相同,所以性能相同 | |
| B. | 镁铝合金可用于制造飞机、汽车等部件 | |
| C. | 铜合金具有优异的导电、导热性能,但耐腐蚀性能力较差 | |
| D. | 铝铁合金具有很高的熔点,能用于制造火箭外层材料. |
 热化学方程式中的H实际上是热力学中的一个物理量,叫做焓.一个体系的焓(H)的绝对值到目前为止还没有办法测得,但当体系发生变化时,我们可以测得体系的焓的变化,即焓变,用“△H”表示,△H=H(终态)-H(始态).
热化学方程式中的H实际上是热力学中的一个物理量,叫做焓.一个体系的焓(H)的绝对值到目前为止还没有办法测得,但当体系发生变化时,我们可以测得体系的焓的变化,即焓变,用“△H”表示,△H=H(终态)-H(始态).