题目内容
某温度下,纯水中c(H+)=3.0×10-7 mol/L,则此时c (OH-)= ;温度不变,向水中滴入盐酸使c(H+)=3.0mol/L,则溶液中c (OH-)= .
【答案】分析:纯水中,氢离子浓度等于氢氧根离子浓度,温度不变,水的离子积常数不变,根据水的离子积常数及氢离子浓度计算氢氧根离子浓度.
解答:解:纯水中c(H+)=c (OH-)=3.0×10-7 mol/L,则KW=c(H+).c (OH-)=(3.0×10-7 mol/L)2=9×10-14 (mol/L)2,
温度不变,水的离子积常数不变,c(H+)=3.0mol/L,则溶液中c (OH-)=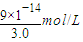 =3.0×10-14 mol/L,
=3.0×10-14 mol/L,
故答案为:3.0×10-7 mol/L;3.0×10-14 mol/L.
点评:本题考查水的离子积常数的有关计算,明确水的离子积常数与温度的关系即可解答,难度不大.
解答:解:纯水中c(H+)=c (OH-)=3.0×10-7 mol/L,则KW=c(H+).c (OH-)=(3.0×10-7 mol/L)2=9×10-14 (mol/L)2,
温度不变,水的离子积常数不变,c(H+)=3.0mol/L,则溶液中c (OH-)=
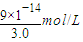 =3.0×10-14 mol/L,
=3.0×10-14 mol/L,故答案为:3.0×10-7 mol/L;3.0×10-14 mol/L.
点评:本题考查水的离子积常数的有关计算,明确水的离子积常数与温度的关系即可解答,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在温度不变时,水溶液中c(H+)和c(OH-)不能同时增大 | B、pH=0的溶液是酸性最强的溶液 | C、强酸的水溶液中不存在OH- | D、某温度下,纯水中c(H+)=2×10-7mol?L-1,其呈酸性 |
 H++CN-、H2O
H++CN-、H2O H++OH-、CN-+H2O
H++OH-、CN-+H2O HCN+OH-
HCN+OH-