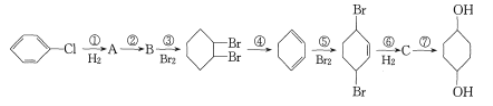
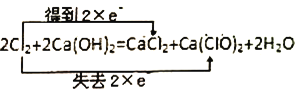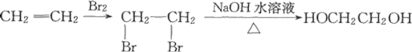��Ŀ����
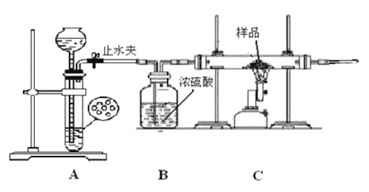
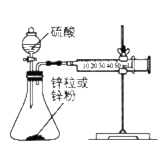
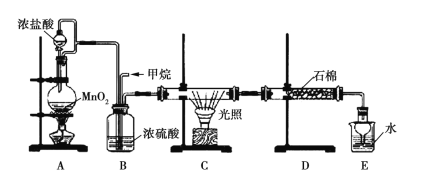
����Ŀ��ij��ѧ�С���������ͼ��ʾ(���ּг�װ������ȥ)ʵ��װ��,��̽����ʪ��Cl2��Na2CO3��Ӧ�õ��Ĺ������ʡ�
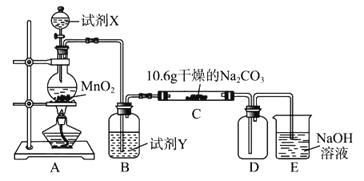
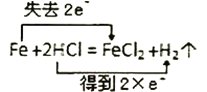
(1)д��װ��A�з�����Ӧ�Ļ�ѧ����ʽ:__________________________________��
(2)д���Լ�Y������:___________________��
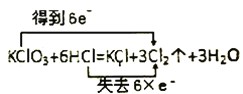
(3)��֪:ͨ��һ�������������D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ�����壬��Ϊ�������������ȷ������C�к��е�����ֻ��һ�֣��Һ���NaHCO3���ֶ�C�ɷֽ��в����̽����
������������衣
����һ:�������ֳɷ�: NaHCO3��___________;
�����:�������ֳɷ�: NaHCO3��___________��_____________��
����Ʒ���,����ʵ�顣��д��ʵ�鲽���Լ�Ԥ������ͽ���(�ɲ�����)��
��ѡʵ���Լ�������:����ˮ��ϡ���ᡢBaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���
ʵ�鲽�� | Ԥ������ͽ��� |
����1��ȡC�е�����������Ʒ���Թ��У��μ���������ˮ�������ܽ⣬Ȼ��������Һ�ֱ�����A��B�Թ��С� | |
����2��_____________________ | ____________ |
����3��__________ | _______________ |
(4)��֪C����0.1 mol Cl2�μӷ�Ӧ��������һ����,����֪C�з�Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
���𰸡�4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O ����ʳ��ˮ(���Ȼ�����Һ) NaCl NaCl Na2CO3 ��A�Թ��еμ�BaCl2��Һ ��������������֤�������в���̼���Ƣ�����Һ����ǣ�֤�������к�̼���� ��B�Թ��еμӹ�����ϡ���ᣬ�ٵμ�AgNO3��Һ ����Һ����ǣ���ϲ���2�еĢ٣������1��������ϲ���2�еĢڣ������2���� 2Cl2+2 Na2CO3+H2O = 2NaHCO3+2NaCl+Cl2O
MnCl2+Cl2��+2H2O ����ʳ��ˮ(���Ȼ�����Һ) NaCl NaCl Na2CO3 ��A�Թ��еμ�BaCl2��Һ ��������������֤�������в���̼���Ƣ�����Һ����ǣ�֤�������к�̼���� ��B�Թ��еμӹ�����ϡ���ᣬ�ٵμ�AgNO3��Һ ����Һ����ǣ���ϲ���2�еĢ٣������1��������ϲ���2�еĢڣ������2���� 2Cl2+2 Na2CO3+H2O = 2NaHCO3+2NaCl+Cl2O
��������
��1��ʵ�����Ʊ����������װ�÷�����֪�����ö������̺�Ũ������ȷ�Ӧ��ȡ������
��2��ʵ�����Ʊ������к����Ȼ��⣬��Ҫ�ñ���ʳ��ˮ��ȥ�Ȼ��⡣
��3��D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ��������֪�Ǻ��ȵ���������ȵ��������У���Ϊ���ۣ���̼�Ļ��ϼ�û�б仯�����Է�Ӧ��Ӧ�и��۵��ȵĻ��������ɣ���������NaCl��C�к���NaHCO3�����п�����δ��ȫ��Ӧ��̼���ƣ��ݴ˿��Եõ�C�ɷֵ����ֲ��롣����2����A�Թ��еμ������Ȼ�����Һ���Ǽ���������Ƿ���̼���ơ�����3Ӧ�Ǽ��������ӣ�Ӧ��B�Թ��еμӹ�����ϡ���ᣬ�ٵμ���������Һ������Һ����ǣ�֤�����庬���Ȼ��ơ�
��4��������һ��������ӦΪ������̼���Ʒ�Ӧ����̼�����ƺ��Ȼ��ƺ�ij���ʣ�����������ԭ��Ӧ�����غ�����жϣ���Ԫ�ػ��ϼ�Ϊ+1��������֪��Ӧ�ɵĺ���������Ϊһ�������ȡ�
��1��ʵ�����Ʊ����������װ�÷�����֪�����ö������̺�Ũ������ȷ�Ӧ��ȡ��������Ӧ�����Ȼ��̺�������ˮ���ʴ�Ϊ4HCl(Ũ)+MnO2![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
��2��ʵ�����Ʊ������к����Ȼ��⣬��Ҫ�ñ���ʳ��ˮ��ȥ�Ȼ��⡣
��3����װ��C��ͨ��һ�������������������ȵ���������������������֪����C�к���Ԫ�ص���ΪNaCl���Һ���̼�����ƣ�����������ֳɷ֣�Ϊ̼�����ƺ��Ȼ��ƣ�����������ֳɷ֣�Ӧ����Ϊ��ȫ��Ӧ��̼���ƣ���̼���ƣ�̼�����ƣ��Ȼ��ơ�����2����A�Թ��еμ������Ȼ�����Һ���Ǽ���������Ƿ���̼���ƣ��ش��С��ʱҪ������Ľ��ۣ�aӦΪ֤�������в�����̼���ƣ�bӦΪ֤�������к���̼���ƣ����ܵߵ�������3Ӧ�Ǽ��������ӣ�Ӧ��B�Թ��еμӹ�����ϡ���ᣬ�ٵμ���������Һ������Һ����ǣ�֤�����庬���Ȼ��ơ�
��4��������һ��������ӦΪ������̼���Ʒ�Ӧ����̼�����ƺ��Ȼ��ƺ�ij���ʡ�10.6gNa2CO3�����ʵ���Ϊ0.1mol��C����0.1 molCl2�μӷ�Ӧ������̼�غ㣬�������е�NaHCO3�����ʵ���ҲΪ0.1mol���ٸ������غ㣬NaCl�����ʵ���ҲΪ0.1mol��0.1molCl2�е�0�۵��ȵĻ��ϼ۽��͵�0.1molNaCl�е�-1�ۣ��õ���0.1mol���ӣ�������0.05molCl2�����ݵ����غ㣬ʣ���0.05molCl2�е�0.1molCl�Ļ��ϼ�Ӧ�����ߵ�+1�ۣ��������ɵ��ȵ�������ΪCl2O����ƽ�Ļ�ѧ����ʽΪ2Cl2+2 Na2CO3+H2O = 2NaHCO3+2NaCl+Cl2O��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��2019��ŵ������ѧ������Լ�����ŵ��ɷ�˹̹������͢���ͼ�Ұ�ã��������Ƕ�����ӵ���о��Ĺ��ס���������ﮣ�LiFePO4�����������Դ�����Ķ������֮һ������ʪ��ұ���ջ��շϾ���������﮵������Ƭ����LiFePO4�⣬������Al�����������������ĵ�������е���Դ������������ͼ��
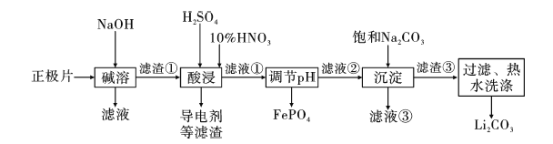
��֪��KSP ( Li2CO3)=2.0��10-3 ���������ʵ��ܽ�ȣ�S�����±���ʾ��
T�� | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
20 | 1.33 | 34.2 | 0.039 |
80 | 0.85 | 30.5 | ���� |
100 | 0.72 | ���� |
��1�� ������������ˮϴ������ԭ����____________��
��2��д������ʱAl���ܽ�Ļ�ѧ����ʽ ___________��
��3�����ʱ����H2O2����HNO3���ã����ŵ���________��
��4����������﮵���ڹ���ʱ����������LiFePO4��FePO4��ת�����õ�طŵ�ʱ�����ĵ缫��ӦʽΪ____��
��5������Һ����c(Li+)=4mol/L������������Na2CO3��Һ��Li+�ij����ʴﵽ90%��������Һ����c(CO32-)=____mol/L