题目内容
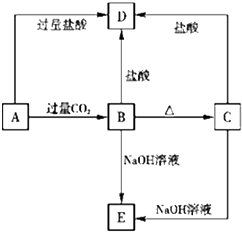 A、B、C、D、E五种化合物,均含有前18号元素中某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).
A、B、C、D、E五种化合物,均含有前18号元素中某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).(1)写出化学式:A
(2)写出下列反应的离子方程式:B→D
考点:无机物的推断
专题:推断题
分析:B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片),说明A中含有K元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2,结合对应物质的性质解答该题.
解答:
解:B、C都既能与盐酸反应又能与NaOH溶液反应,应为两性化合物,因B加热分解可生成C,则可知B为Al(OH)3,C为A12O3,则D为AlCl3,E为NaAlO2,若取A溶液灼烧,焰色反应为紫色(透过蓝色钴玻璃片),说明A中含有K元素,A能与二氧化碳反应生成Al(OH)3,则A应为KAlO2,
(1)通过以上分析知,A、B、C、D分别是KAlO2、Al(OH)3、A12O3、AlCl3,
故答案为:KAlO2;Al(OH)3;A12O3;AlCl3;
(2)B→D为Al(OH)3生成AlCl3的反应,离子方程式为Al(OH)3+3H+=Al3++3H2O,C→E为A12O3生成NaAlO2的反应,离子方程式为A12O3+2OH-=2A1O2-+H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;A12O3+2OH-=2A1O2-+H2O.
(1)通过以上分析知,A、B、C、D分别是KAlO2、Al(OH)3、A12O3、AlCl3,
故答案为:KAlO2;Al(OH)3;A12O3;AlCl3;
(2)B→D为Al(OH)3生成AlCl3的反应,离子方程式为Al(OH)3+3H+=Al3++3H2O,C→E为A12O3生成NaAlO2的反应,离子方程式为A12O3+2OH-=2A1O2-+H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;A12O3+2OH-=2A1O2-+H2O.
点评:本题考查了铝及其化合物之间的转化,根据B能和强酸、强碱反应且加热易分解推断知,B是氢氧化铝,再结合物质的反应条件、反应物来分析解答,难度中等.

练习册系列答案
相关题目
下列气体不能用排空气法收集的是( )
| A、NH3 |
| B、Cl2 |
| C、NO2 |
| D、NO |
氯在自然界以化合物形态存在,18世纪70年代,首先发现并制得氯气的化学家是( )
| A、汤姆生 | B、舍勒 |
| C、阿伏加德罗 | D、戴维 |
关于酚羟基和醇羟基的分析中,错误的是( )
| A、原子组成一样 |
| B、O-H键的化学键类型一样 |
| C、羟基中氢原子活性性不同 |
| D、酚羟基能发生电离,醇羟基也能发生电离 |
物质对应的用途(括号内是用途)错误的是( )
| A、单质硅(光导纤维) |
| B、钠钾合金(原子反应堆导热剂) |
| C、过氧化钠(潜水艇中供氧剂) |
| D、硫酸钡(医疗钡餐) |
向含有Cu(NO3)2,Zn(NO3)2,Fe(NO3)3,AgNO3各0.1mol的混合溶液中加入0.1mol铁粉,充分搅拌反应后,下列结论错误的是( )
| A、溶液中析出0.05mol Cu |
| B、溶液中析出0.1mol Ag |
| C、溶液中Cu2+与Fe2+的浓度之比为1:2 |
| D、往反应后的溶液中再加入0.1mol 铁粉,铁粉恰好完全溶解 |
下列物质中,属于电解质的是( )
| A、NaOH | B、蔗糖 |
| C、稀盐酸 | D、NaCl溶液 |

 (苯胺,弱碱性、易氧化)
(苯胺,弱碱性、易氧化)

