题目内容
【题目】有关下图所示化合物的说法不正确的是 ( ) 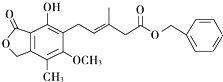
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
【答案】D
【解析】解:A、有机物含有碳碳双键,故可以与Br2发生加成反应,又含有甲基,故可以与Br2光照发生取代反应,故A正确;
B、酚羟基要消耗一个NaOH,两个酯基要消耗两个NaOH,1mol该化合物最多可以与3molNaOH反应,故B正确;
C、苯环可以催化加氢,碳碳双键可以使KMnO4褪色,故C正确;
D、该有机物中不存在羧基,并且酚羟基酸性比碳酸弱,故不能与NaHCO3放出CO2气体,故D错误.
故选D.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目