题目内容
20.将铁片加到1L 1mol/L三氯化铁溶液中,当亚铁离子和铁离子的浓度相等时,铁片的质量减少( )| A. | 2.8g | B. | 5.6g | C. | 11.2g | D. | 1.4g |
分析 铁粉放入三氯化铁溶液中发生反应Fe+2Fe3+=3Fe2+,已反应的Fe3+的物质的量为1mol,根据方程式计算生成的Fe2+的物质的量,进而得到未反应的Fe3+的物质的量,二者之比即为答案.
解答 解:设参加反应的铁为xmol,则:
Fe+2Fe3+=3Fe2+
xmol 2xmol 3xmol
溶液中的Fe3+和Fe2+浓度相等,即1-2x=3x,所以x=0.2mol,
反应的铁的质量为:0.2mol×56g/mol=11.2g,
故选C.
点评 本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高频考点,注意结合反应的离子方程式计算该题,难度不大.

练习册系列答案
相关题目
10.A、B、C、D、E 是同一短周期的五种元素,A和B的最高价氧化物对应的水化物呈碱性,且碱性A强于B,C和D的最高价氧化物的水溶液呈酸性,且酸性C强于D,五种元素形成的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序( )
| A. | CDEBA | B. | ECDAB | C. | BAEDC | D. | CDBAE |
5.下表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的名称碳,氮;⑧、⑨两种元素的符号SiP.
(2)在这些元素中,Na(用元素符号填写,下同)是最活泼的金属元素;F是最活泼的非金属元素.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)写出①的最高价氧化物的化学式CO2
(5)比较⑤与⑥的化学性质,Na更活泼.
| 周期/族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,Na(用元素符号填写,下同)是最活泼的金属元素;F是最活泼的非金属元素.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)写出①的最高价氧化物的化学式CO2
(5)比较⑤与⑥的化学性质,Na更活泼.
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,22.4L乙烯中C-H键数为4NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
9.表示一个原子在第三个电子层上有10个电子可以写成( )
| A. | 3s10 | B. | 3d10 | C. | 3s23p63d2 | D. | 3s23p53d3 |
10.烯烃R-CH═CH-R′在过量的酸性高锰酸钾溶液存在下,可氧化成RCOOH和R′COOH.现有分子式为C6H12的链烃,用过量的酸性高锰酸钾氧化生成两种不同的羧酸,则该烃的结构简式为(己知R′≠H)( )
| A. | CH2═CH-CH2CH2CH2CH3 | B. | CH3CH2CH═CHCH2CH3 | ||
| C. | CH3CH═CHCH2CH2CH3 | D. | 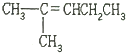 |
 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
 CH3COOC2H5+H2O,反应类型酯化反应(取代反应).
CH3COOC2H5+H2O,反应类型酯化反应(取代反应).