题目内容
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 常温常压下,22.4L乙烯中C-H键数为4NA | |
| B. | 1L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
分析 A.常温常压下,气体摩尔体积大于22.4L/mol;
B.乙酸是弱酸,不能完全电离;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数;
D.标准状况甲醇不是气体.
解答 解:A.常温常压下,气体摩尔体积大于22.4L/mol,故A错误;
B.乙酸是弱酸,不能完全电离;1L0.1mol•L-1乙酸溶液中H+数小于0.1NA,故B正确;
C.乙烯和丁烯的最简式为CH2,只需计算21.0gCH2中碳原子数═$\frac{21g}{14g/mol}$×NA=1.5NA,标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA ,故C正确;
D.标准状况甲醇不是气体,22.4L甲醇物质的量不是1mol,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用概念理解,微粒数计算,气体摩尔体积的条件应用,物质性质的分析判断是解题关键.题目难度中等.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
3.下列产品或材料属于复合材料的是( )
①玻璃钢
②采用碳纤维增强复合材料制的钓鱼竿
③航天飞机机身
④航天飞机隔热陶瓷瓦
⑤纳米高分子复合材料.
①玻璃钢
②采用碳纤维增强复合材料制的钓鱼竿
③航天飞机机身
④航天飞机隔热陶瓷瓦
⑤纳米高分子复合材料.
| A. | ①⑤ | B. | ①②③④⑤ | C. | ②⑤ | D. | ①②③ |
20.将铁片加到1L 1mol/L三氯化铁溶液中,当亚铁离子和铁离子的浓度相等时,铁片的质量减少( )
| A. | 2.8g | B. | 5.6g | C. | 11.2g | D. | 1.4g |
7.下列物质的分类合理的是( )
| A. | 盐:Ca(ClO)2 NH4NO3 K2SiO3 | |
| B. | 酸性氧化物:Al2O3 K2O CO2 | |
| C. | 电解质:HCl Ba(OH)2 CO | |
| D. | 非电解质:Cl2 NO 乙醇(C2H5OH) |
17.磷酸分子间脱水会形成多种聚磷酸,它们的钠盐是广泛使用的食品添加剂.将48gNaOH与58.8g固态纯H3PO4在一定温度下加热,得到79.8g固体A和27g水,则A可能是( )
| A. | Na3PO4 | B. | Na3PO3 | ||
| C. | Na4P2O7 和Na5P3O10 | D. | Na3PO4、Na4P2O7和Na5P3O10 |
4.Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小(不包括稀有气体),R、X、Y三种元素的原子核外电子层数相同,同一周期中R的一种单质的熔点最高,Y与Q、R、X、Z均能形成多种常见化合物.下列说法正确的是( )
| A. | X.Y形成的最简单化合物的稳定性:X>Y | |
| B. | Z位于元素周期表的第三周期第IA族 | |
| C. | Q与R两元素组成的分子构型是正四面体型 | |
| D. | X、Y最多可以形成5种化合物 |
1.下列关于物质的分离,提纯实验中的一些操作或做法,其中正确的是( )
| A. | 在组装蒸馏装置时,温度计的水银球应伸入液面下 | |
| B. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| C. | 要除去乙烷中混有的乙烯气体可将混合气体通过盛有酸性高猛酸钾溶液的洗气瓶 | |
| D. | 用分液漏斗可以分离溴和CCl4、苯和水、乙酸和乙醇等液体混合物 |
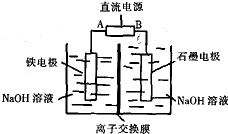 高铁酸钠(Na2FeO4)是一种新型多功能材料,工业上Na2FeO4制备方法是以纯铁棒与石墨电极为工作电极,用有隔膜的电解槽(如图所示),电解浓NaOH溶液制备高铁酸钠,化学方程式为:
高铁酸钠(Na2FeO4)是一种新型多功能材料,工业上Na2FeO4制备方法是以纯铁棒与石墨电极为工作电极,用有隔膜的电解槽(如图所示),电解浓NaOH溶液制备高铁酸钠,化学方程式为: