题目内容
10.下列电子式书写正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 A、HClO为共价化合物,分子中含有1个O-Cl键和个H-O键;
B、氯原子有7个电子;
C、H2S是共价化合物;
D、过氧化钠由2个钠离子和1个过氧根构成.
解答 解:A、HClO为共价化合物,分子中含有1个O-Cl键和个H-O键,其电子式为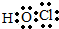 ,故A错误;
,故A错误;
B、氯原子有7个电子,故四氯化碳的电子式为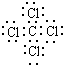 ,故B错误;
,故B错误;
C、H2S是共价化合物,硫原子满足8电子稳定结构,故电子式为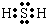 ,故C错误;
,故C错误;
D、过氧化钠由2个钠离子和1个过氧根构成,钠离子的电子式是其离子符号本身,过氧根中两个氧原子形成一对共用电子对,故电子式为 ,故D正确.
,故D正确.
故选D.
点评 本题考查了常见的化学用语,难度不大,应注意的是在书写电子式之前应先判断化合物的类型.

练习册系列答案
相关题目
20.下列物质中只含共价键的是( )
| A. | Na2O2 | B. | NH4Cl | C. | H2O2 | D. | Ba(OH)2 |
1.下列各化合物的命名正确的是( )
| A. | C(CH3)4 1,1,2,2-四甲基甲烷 | |
| B. |  1,3,4-三甲苯 1,3,4-三甲苯 | |
| C. | CH3CH2CH(OH)CH3 2-丁醇 | |
| D. | CH3CH2CH2Br 溴丙烷 |
18. 我国科学工作者合成了许多结构复杂的天然有机化合物,如叶绿素、血红素、维生素B12等.叶绿素的结构如图.下列有关说法中正确的是( )
我国科学工作者合成了许多结构复杂的天然有机化合物,如叶绿素、血红素、维生素B12等.叶绿素的结构如图.下列有关说法中正确的是( )
 我国科学工作者合成了许多结构复杂的天然有机化合物,如叶绿素、血红素、维生素B12等.叶绿素的结构如图.下列有关说法中正确的是( )
我国科学工作者合成了许多结构复杂的天然有机化合物,如叶绿素、血红素、维生素B12等.叶绿素的结构如图.下列有关说法中正确的是( )| A. | 叶绿素属于高分子化合物 | |
| B. | 在一定条件下,叶绿素能发生加成、水解、酯化等反应 | |
| C. | 叶绿素分子中含有两种类型的双键 | |
| D. | 叶绿素中Mg2+与四个N之间结合方式不完全相同 |
5.如图是某有机物的球棍模型,下列关于该有机物的性质叙述中错误的是( )


| A. | 该有机物的分子式为C9H11O2N | B. | 能合成高分子化合物 | ||
| C. | 能发生加成反应 | D. | 能发生水解反应 |
15.某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g.
请完成以下实验设计表,并在实验目的一栏中填空:
(Ⅱ)把2.5mol A和2.5mol B混合放入2L密闭容器里,发生反应:3A(g)+B(g)?xC(g)+2D(g),经5s后反应达平衡.在此5s内C的平均反应速率为0.2mol/(L•s),同时生成1mol D.试求:
(1)达平衡时B的转化率为20%.
(2)x的值为4.
(3)若温度不变,达平衡时容器内气体的压强是反应前的1.2倍.
请完成以下实验设计表,并在实验目的一栏中填空:
| 实验 编号 | 温度 (℃) | 大理石 规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究固体物质的表面积对反应速率的影响 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
(1)达平衡时B的转化率为20%.
(2)x的值为4.
(3)若温度不变,达平衡时容器内气体的压强是反应前的1.2倍.
20.分别将下列各物质等体积混合,在室温下剧烈振荡,静置后能形成均匀溶液的是( )
| A. | 乙酸乙酯 水 | B. | 苯 水 | C. | 乙醇 水 | D. | 四氯化碳 碘水 |