题目内容
下列说法不正确的是( )
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、水解反应NH4++H2O?NH3?H2O+H+达到平衡后,升高温度平衡逆向移动 |
| C、制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D、盐类水解反应的逆反应是中和反应 |
考点:盐类水解的原理,胶体的应用
专题:
分析:A、明矾溶液中铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用;
B、水解过程是吸热反应,升温平衡正向进行;
C、AlCl3、FeCl3、CuCl2溶液中金属阳离子水解,生成的产物中都生成氯化氢,加热氯化氢挥发得到水解产物;
D、盐类水解是中和反应的逆反应;
B、水解过程是吸热反应,升温平衡正向进行;
C、AlCl3、FeCl3、CuCl2溶液中金属阳离子水解,生成的产物中都生成氯化氢,加热氯化氢挥发得到水解产物;
D、盐类水解是中和反应的逆反应;
解答:
解:A、明矾溶液中铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以做净水剂,故A正确;
B、水解过程是吸热反应,水解反应NH4++H2O?NH3?H2O+H+达到平衡后,升温平衡正向进行,故B错误;
C、AlCl3、FeCl3、CuCl2溶液中金属阳离子水解,生成的产物中都生成氯化氢,加热氯化氢挥发得到水解产物金属的氢氧化物沉淀,制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法,故C正确;
D、盐类水解是中和反应的逆反应,故D正确;
故选B.
B、水解过程是吸热反应,水解反应NH4++H2O?NH3?H2O+H+达到平衡后,升温平衡正向进行,故B错误;
C、AlCl3、FeCl3、CuCl2溶液中金属阳离子水解,生成的产物中都生成氯化氢,加热氯化氢挥发得到水解产物金属的氢氧化物沉淀,制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法,故C正确;
D、盐类水解是中和反应的逆反应,故D正确;
故选B.
点评:本题考查了盐类水解的分析判断,水解过程,水解产物的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
与氢气完全加成后,能生成2-甲基丁烷的烃是( )
| A、CH2=CH-CH2-CH3 |
| B、CH2=C(CH3) CH=CH2 |
| C、(CH3)2CHCH=CH2 |
| D、(CH3)3CCH═CH2 |
在2NO2?N2O4的可逆反应中,下列状态属于平衡状态的是( )
| A、υ正=υ逆≠0时的状态 |
| B、NO2全部转变成N2O4的状态 |
| C、c(NO2)=c(N2O4)的状态 |
| D、气体的质量不再发生变化的状态 |
下列实验能达到目的是( )
| A、在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸 |
| B、蒸馏操作时在蒸馏烧瓶中加入沸石以防止爆沸 |
| C、用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D、加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
某学习小组设计有关Na2CO3和Na2HCO3的探究实验,其中设计方案明显错误的是( )
| A、可用加热的方法除去Na2CO3固体中混有Na2HCO3 |
| B、可向Na2HCO3溶液中通入过量的CO2气体除去其中混有的Na2CO3 |
| C、可用澄清石灰水鉴别Na2HCO3和Na2CO3两种溶液 |
| D、分别向Na2CO3溶液、Na2HCO3溶液中滴加过量的稀盐酸,均有气泡产生 |
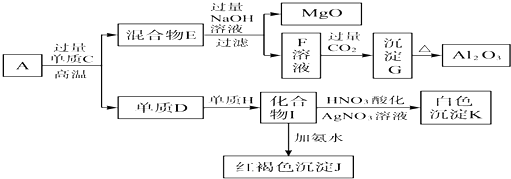
 A、B、C、D、E代表单质或化合物,它们之间的相互转化关系如图所示.A为地壳中含量仅次于氧的非金属单质,其晶体结构与金刚石相似.
A、B、C、D、E代表单质或化合物,它们之间的相互转化关系如图所示.A为地壳中含量仅次于氧的非金属单质,其晶体结构与金刚石相似. 如图物质的转化关系中,A为难熔固体单质,E为一种白色不溶物,a是焰色反应呈黄色的强碱溶液.据此回答:
如图物质的转化关系中,A为难熔固体单质,E为一种白色不溶物,a是焰色反应呈黄色的强碱溶液.据此回答: