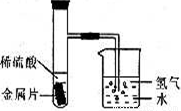
Ⅰ某自然科学兴趣小组设计了如下图所示的装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同溶质质量分数的稀硫酸反应,观察在30s里从导管口冒出的氢气泡多少,记录在下表中.(“+”越多表示产生的气泡越多)
(1)从实验结果可看出,甲、乙、丙、丁四种金属与稀硫酸反应由快到慢的顺序是______
(2)如果四种金属分别是镁、铝、铁、锌中的一种,则丁最有可能是______
Ⅱ甲同学为了探究铝、铁和铜三种金属的活动性,他用铜丝、铁丝、铝丝和稀盐酸四种物质,设计了以下只用一支试管,取一次盐酸的探究方案.
请你帮助甲同学完善下表中的探究方案.
结论:金属活动性______写出①中反应的化学方程式:______.
| 金属 | 甲 | 乙 | 丙 | 丁 |
| 氢气泡的多少 | ++ | ++++ | +++ | + |
(2)如果四种金属分别是镁、铝、铁、锌中的一种,则丁最有可能是______
Ⅱ甲同学为了探究铝、铁和铜三种金属的活动性,他用铜丝、铁丝、铝丝和稀盐酸四种物质,设计了以下只用一支试管,取一次盐酸的探究方案.
请你帮助甲同学完善下表中的探究方案.
| 实验步骤 | 实验现象 |
| ①在试管里取少量盐酸,插入铁丝,充分作用 | 溶液由无色变为浅绿色,有大量气体生成 |
| ②在①所得的溶液中,插入______,充分作用 | 无明显现象 |
| ③在②所得溶液中,插入______,充分作用 | 金属铝表面有一层,黑色物质生成 |

现有铜与铁的混合物粉末现欲测定其组成.取该混合物粉末10.0g放入烧杯中,将140.0g稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
通过计算(写出计算过程),求:
(1)混合粉末中铜粉的质量为______g
(2)求所用稀硫酸的溶质的质量分数.(写出计算过程)
(3)第三次加完稀硫酸反应后所得溶液中溶质的质量分数为______(不要求写出计算过程)
0 84738 84746 84752 84756 84762 84764 84768 84774 84776 84782 84788 84792 84794 84798 84804 84806 84812 84816 84818 84822 84824 84828 84830 84832 84833 84834 84836 84837 84838 84840 84842 84846 84848 84852 84854 84858 84864 84866 84872 84876 84878 84882 84888 84894 84896 84902 84906 84908 84914 84918 84924 84932 211419
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 7.2 | 4.4 | 1.6 | 1.6 |
(1)混合粉末中铜粉的质量为______g
(2)求所用稀硫酸的溶质的质量分数.(写出计算过程)
(3)第三次加完稀硫酸反应后所得溶液中溶质的质量分数为______(不要求写出计算过程)



