题目内容
某同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:(1)当加入K2CO3溶液的质量为______ g时,原混合溶液中的盐酸恰好被反应完全.
(2)原混合溶液中氯化钙的质量是多少?(写出计算过程)
(3)恰好完全反应时所得溶液中溶质的质量分数为______.

【答案】分析:根据图象信息可知10克之前没有出现沉淀,所以和盐酸反应的碳酸钾是10克,当加入K2CO3溶液的质量为10g时,原混合溶液中的盐酸恰好被反应完全;
根据与20g13.8%的碳酸钾溶液反应生成2克沉淀,可求出氯化钙的质量;
根据碳酸钾会与盐酸反应生成二氧化碳气体,碳酸钾会与氯化钙生成碳酸钙沉淀,溶液质量等于加入的总质量减去生成的气体和沉淀的质量,溶质的质量分别为碳酸钾与盐酸反应生成的氯化钾的质量加上氯化钙与碳酸钾反应生成的氯化钾的质量,即可求出溶质的质量分数.
解答:解:(1)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾是10克,当加入K2CO3溶液的质量为10g时,原混合溶液中的盐酸恰好被反应完全;
(2)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾是10克,从10开始出现沉淀,到30沉淀不变,说明和氯化钙反应的碳酸钾是20克,生成沉淀是2克,设碳酸钾和盐酸反应生成的氯化钾质量为y,生成的二氧化碳的质量为x
K2CO3+2HCl=2KCl+H2O+CO2↑
138 149 44
10g×13.8% y x
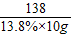 =
=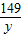 =
=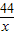
x=0.44g y=1.49g
设和碳酸钾反应的氯化钙为a,生成氯化钾为b,生成的碳酸钙质量为c
K2CO3+CaCl2=2KCl+CaCO3↓
138 111 149 100
20g×13.8% a b c
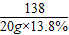 =
=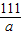 =
=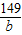 =
=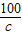
a=2.22克 b=2.98克 c=2g
答:原混合溶液中CaCl2的质量为2.22g.
(2)反应后烧杯中的物质包括两个反应中生成的氯化钾,其质量为:1.49g+2.98g=4.47g,恰好完全反应时滴入的碳酸钾的质量为30g,故反应后溶液的质量
为:30g+40g-2g-0.44g=67.56g,则恰好完全反应后,溶液中溶质的质量分数为: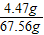 ×100%=6.61%
×100%=6.61%
答:恰好完全反应时所得溶液中溶质的质量分数为6.61%.
点评:在解此类题时,首先根据图象分析反应的原理,然后再根据题中的条件利用方程式进行求解.最后的固体求酸注意要包含碳酸钙,因为题干要求的是烧杯内的物质.
根据与20g13.8%的碳酸钾溶液反应生成2克沉淀,可求出氯化钙的质量;
根据碳酸钾会与盐酸反应生成二氧化碳气体,碳酸钾会与氯化钙生成碳酸钙沉淀,溶液质量等于加入的总质量减去生成的气体和沉淀的质量,溶质的质量分别为碳酸钾与盐酸反应生成的氯化钾的质量加上氯化钙与碳酸钾反应生成的氯化钾的质量,即可求出溶质的质量分数.
解答:解:(1)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾是10克,当加入K2CO3溶液的质量为10g时,原混合溶液中的盐酸恰好被反应完全;
(2)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾是10克,从10开始出现沉淀,到30沉淀不变,说明和氯化钙反应的碳酸钾是20克,生成沉淀是2克,设碳酸钾和盐酸反应生成的氯化钾质量为y,生成的二氧化碳的质量为x
K2CO3+2HCl=2KCl+H2O+CO2↑
138 149 44
10g×13.8% y x
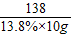 =
=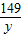 =
=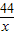
x=0.44g y=1.49g
设和碳酸钾反应的氯化钙为a,生成氯化钾为b,生成的碳酸钙质量为c
K2CO3+CaCl2=2KCl+CaCO3↓
138 111 149 100
20g×13.8% a b c
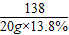 =
=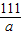 =
=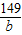 =
=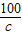
a=2.22克 b=2.98克 c=2g
答:原混合溶液中CaCl2的质量为2.22g.
(2)反应后烧杯中的物质包括两个反应中生成的氯化钾,其质量为:1.49g+2.98g=4.47g,恰好完全反应时滴入的碳酸钾的质量为30g,故反应后溶液的质量
为:30g+40g-2g-0.44g=67.56g,则恰好完全反应后,溶液中溶质的质量分数为:
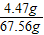 ×100%=6.61%
×100%=6.61%答:恰好完全反应时所得溶液中溶质的质量分数为6.61%.
点评:在解此类题时,首先根据图象分析反应的原理,然后再根据题中的条件利用方程式进行求解.最后的固体求酸注意要包含碳酸钙,因为题干要求的是烧杯内的物质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2013?常州)使用如图所示装置制取氧气.
(2013?常州)使用如图所示装置制取氧气.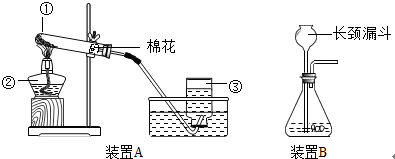
 通过化学课程的学习,我们收获很多.
通过化学课程的学习,我们收获很多.

 了如表所示的系列实验:
了如表所示的系列实验: