回答下列问题.
(1)铁在食品防腐上有重要的作用.为防止月饼变质,常在内包装中放入一小包防腐剂,其主要成分是铁粉.铁粉的作用是 .
(2)将锌粉加入到由AgNO3和Cu(NO3)2组成的一定质量的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为 ,滤液中的溶质是 .
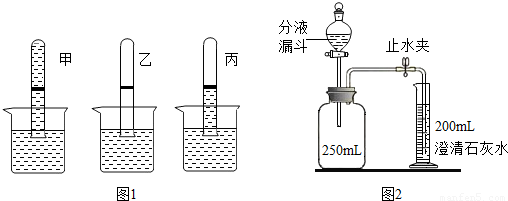
(3)用如图所示装置进行下列实验,向“人”字型管的甲、乙两端分别装入适量表中所示物质,并进行相应操作,填写下表.

0 83906 83914 83920 83924 83930 83932 83936 83942 83944 83950 83956 83960 83962 83966 83972 83974 83980 83984 83986 83990 83992 83996 83998 84000 84001 84002 84004 84005 84006 84008 84010 84014 84016 84020 84022 84026 84032 84034 84040 84044 84046 84050 84056 84062 84064 84070 84074 84076 84082 84086 84092 84100 211419
(1)铁在食品防腐上有重要的作用.为防止月饼变质,常在内包装中放入一小包防腐剂,其主要成分是铁粉.铁粉的作用是 .
(2)将锌粉加入到由AgNO3和Cu(NO3)2组成的一定质量的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为 ,滤液中的溶质是 .
(3)用如图所示装置进行下列实验,向“人”字型管的甲、乙两端分别装入适量表中所示物质,并进行相应操作,填写下表.
| 甲中的物质 | 乙中的物质 | 操 作 | 现 象 |
| 饱和石灰水 | 浓硫酸 | 盖上塞子,较长时间后 | ① |
| 碳酸钠溶液 | 盖上塞子,倾斜装置,使乙中液体流入甲中 | ② | |
| 少量碳酸钙固体 | 向乙中滴入少量稀盐酸后盖上塞子 | ③ | |
| 底部有少量KNO3固体的KNO3溶液 | 将甲、乙两端同时放入热水中 | ④ | |
| ⑤甲中 | 乙中 | 倾斜装置,使乙中液体流入甲中 | 甲中有无色气泡产生 |

 2CaSO4;
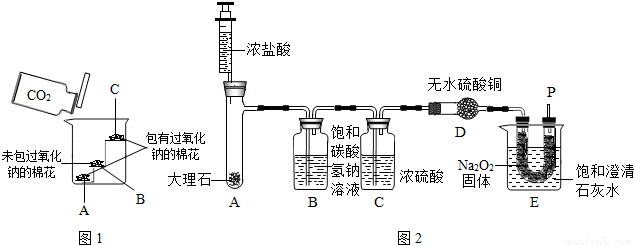
2CaSO4; 工业纯碱中常含有少量的NaCl杂质.右图是测定纯碱样品中Na2CO3质量分数的实验装置(气密性良好,样品质量为11.0g,装置D的质量为172.2g).操作步骤为:将样品装入广口瓶中→打开止水夹,缓缓鼓入空气数分钟→连接装置D→关闭止水夹,向盛有样品的广口瓶中滴加稀硫酸至不再产生气泡→打开止水夹,再缓缓鼓入空气数分钟→称量装置D的质量为176.6g.(假设每套装置均反应完全).
工业纯碱中常含有少量的NaCl杂质.右图是测定纯碱样品中Na2CO3质量分数的实验装置(气密性良好,样品质量为11.0g,装置D的质量为172.2g).操作步骤为:将样品装入广口瓶中→打开止水夹,缓缓鼓入空气数分钟→连接装置D→关闭止水夹,向盛有样品的广口瓶中滴加稀硫酸至不再产生气泡→打开止水夹,再缓缓鼓入空气数分钟→称量装置D的质量为176.6g.(假设每套装置均反应完全).