题目内容
已知A、B、C、D、E、F、G是初中化学常见的物质,(“→”表示物质间存在转化关系.图中已略去部分物质)试回答以下问题.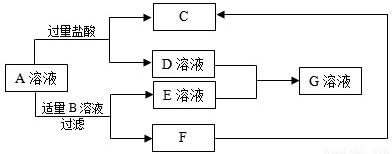
(1)D溶液中的溶质为 .
(2)E溶液中的溶质为 .
(3)向G溶液中滴加无色酚酞试液,若溶液为无色,则G溶液中溶质的所有可能组成为 ;若溶液为红色,则G溶液中溶质的所有可能组成为 .
(4)写出F→C的化学反应方程式 .
【答案】分析:根据物质的化学性质物质进行鉴别,根据常见的物质的性质或相互关系,通过细致地分析、推断,来鉴别出它们究竟是哪一种具体的物质的复杂过程,推断完毕,可代入验证,符合转化关系即可.
解答:解:根据题意:A、B、C、D、E、F、G是初中化学常见物质,图示中CF形成的不是溶液,则二者可能是气体或沉淀,由A加入适量B过滤可知F是沉淀;
A溶液可与盐酸、B溶液反应,则A可能是碱或盐的溶液,若A是碳酸钠溶液,则C是二氧化碳,D溶液中有氯化钠和过量的盐酸;
碳酸钠与氢氧化钙溶液反应可生成碳酸钙沉淀F和氢氧化钠溶液E,碳酸钙高温分解生成二氧化碳C,也可能与盐酸反应生成,D中过量的盐酸与E中氢氧化钠可反应生成氯化钠溶液G;由此推出这几种物质,代入符合物质间的转化关系;
(1)D溶液是碳酸钠溶液与过量盐酸反应生成的氯化钠及过量盐酸的混合溶液;
故答案为:NaCl 和HCl;
(2)碳酸钠与氢氧化钙溶液反应可生成碳酸钙沉淀F和氢氧化钠溶液E;
故答案为:NaOH;
(3)向G溶液中滴加无色酚酞试液,若溶液为无色,说明溶液显中性或酸性;G溶液中可能含有氢氧化钠与盐酸恰好反应生成的氯化钠,还可能含有过量的盐酸;若溶液为红色,说明溶液显碱性,氢氧化钠溶液过量,溶液中含有氯化钠和氢氧化钠;
故答案为:NaCl 或NaCl和HCl; NaOH和NaCl;
(4)碳酸钙与盐酸反应生成二氧化碳、水和二氧化碳,或碳酸钙高温分解生成二氧化碳和氧化钙;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑(合理均可)
其他合理答案也可.
点评:本题重点考查了酸、碱、盐化学性质及其之间的相互转化,有一定难度,解答时结合所学的相关知识和技能,细致分析,探究、推理后,按照题目要求进行认真地选择或解答即可.
解答:解:根据题意:A、B、C、D、E、F、G是初中化学常见物质,图示中CF形成的不是溶液,则二者可能是气体或沉淀,由A加入适量B过滤可知F是沉淀;
A溶液可与盐酸、B溶液反应,则A可能是碱或盐的溶液,若A是碳酸钠溶液,则C是二氧化碳,D溶液中有氯化钠和过量的盐酸;
碳酸钠与氢氧化钙溶液反应可生成碳酸钙沉淀F和氢氧化钠溶液E,碳酸钙高温分解生成二氧化碳C,也可能与盐酸反应生成,D中过量的盐酸与E中氢氧化钠可反应生成氯化钠溶液G;由此推出这几种物质,代入符合物质间的转化关系;
(1)D溶液是碳酸钠溶液与过量盐酸反应生成的氯化钠及过量盐酸的混合溶液;
故答案为:NaCl 和HCl;
(2)碳酸钠与氢氧化钙溶液反应可生成碳酸钙沉淀F和氢氧化钠溶液E;
故答案为:NaOH;
(3)向G溶液中滴加无色酚酞试液,若溶液为无色,说明溶液显中性或酸性;G溶液中可能含有氢氧化钠与盐酸恰好反应生成的氯化钠,还可能含有过量的盐酸;若溶液为红色,说明溶液显碱性,氢氧化钠溶液过量,溶液中含有氯化钠和氢氧化钠;
故答案为:NaCl 或NaCl和HCl; NaOH和NaCl;
(4)碳酸钙与盐酸反应生成二氧化碳、水和二氧化碳,或碳酸钙高温分解生成二氧化碳和氧化钙;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑(合理均可)
其他合理答案也可.
点评:本题重点考查了酸、碱、盐化学性质及其之间的相互转化,有一定难度,解答时结合所学的相关知识和技能,细致分析,探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
 已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质.它们之间相互转化的关系如右图所示(图中反应条件已略去).
已知A、B、C、D、E、F为常见物质,其中A、B含有相同的元素,B、E为氧化物,C、D、F都为单质.它们之间相互转化的关系如右图所示(图中反应条件已略去). (2013?沈阳)已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示.其中A被看作是理想的“绿色能源”,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出)
(2013?沈阳)已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示.其中A被看作是理想的“绿色能源”,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出) 如图已知A、B、C、D、E、F为初中化学常见的物质,六种物质相互反应及转化关系如图:
如图已知A、B、C、D、E、F为初中化学常见的物质,六种物质相互反应及转化关系如图: 已知A、B、C、D、E、F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“
已知A、B、C、D、E、F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“