水在日常生活、工农业生产、科学研究领域有着重要及广泛的用途.
(1)从化学视角看水.从组成角度看,电解水实验证明了水由 组成;从微粒角度看,水由 (填“分子”、“原子”或“离子”)构成.
(2)水能参加许多化学反应.图是一种家用环保型消毒液发生器:原理是电解饱和氯化钠溶液,制得的消毒液有较强的杀菌能力,该反应是利用氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气,该反应的化学方程式为 ;从能量变化角度看,该反应中 转化为化学能.
(3)水是一种重要的溶剂.下表表示的是不同温度下4种盐在水中的溶解度.
回答问题:
①上述4种盐中,30℃时溶解度最大的是 .
②10℃时将16.8gNH4HCO3固体放入100g水中充分溶解,所得溶液为 (填“饱和”或“不饱和”)溶液.
③在20℃时,向含NH4HCO321g的饱和溶液中加入足量食盐.随着食盐的加入,能析出的晶体是 .
A.NH4HCO3 B.NH4Cl C.NaHCO3.

(1)从化学视角看水.从组成角度看,电解水实验证明了水由 组成;从微粒角度看,水由 (填“分子”、“原子”或“离子”)构成.
(2)水能参加许多化学反应.图是一种家用环保型消毒液发生器:原理是电解饱和氯化钠溶液,制得的消毒液有较强的杀菌能力,该反应是利用氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气,该反应的化学方程式为 ;从能量变化角度看,该反应中 转化为化学能.
(3)水是一种重要的溶剂.下表表示的是不同温度下4种盐在水中的溶解度.
| 10℃ | 20℃ | 30℃ | |
| NaCI | 35.8 | 36.0 | 36.3 |
| NH4HCO3 | 15.8 | 21.0 | 27.O |
| NaHCO3 | 8.1 | 9.6 | 11.1 |
| NH4Cl | 33.3 | 37.2 | 41.4 |
①上述4种盐中,30℃时溶解度最大的是 .
②10℃时将16.8gNH4HCO3固体放入100g水中充分溶解,所得溶液为 (填“饱和”或“不饱和”)溶液.
③在20℃时,向含NH4HCO321g的饱和溶液中加入足量食盐.随着食盐的加入,能析出的晶体是 .
A.NH4HCO3 B.NH4Cl C.NaHCO3.

a、b、c、d、e是初中化学中常见的5种元素,有关信息如下表所示.A、B、C、D、E、F、G、H是由上述5种元素中的一种或几种组成的纯净物,其中C、D、F为氧化物.
(1)A的化学式 .
(2)B、C均由a、b元素组成,一定条件下,B可以转化为C,其化学方程式为 .
(3)D与C反应生成E,E与F反应可以生成C和G.则E与F反应的化学方程式为 .
(4)E能转化为H.该反应的化学方程式为 .
(5)A、B、C、D、E、F、G、H 8种物质中能与盐酸反应的是 (写字母序号).
| 元素 | a | b | C | d | e |
| 有关信息 | 其单质A是密度最小的气体 | 地壳中含量最多的元素 | 形成化合物种类最多的元素 | 该元素大量存在于人的骨骼和牙齿中 | 质子数为11 |
(2)B、C均由a、b元素组成,一定条件下,B可以转化为C,其化学方程式为 .
(3)D与C反应生成E,E与F反应可以生成C和G.则E与F反应的化学方程式为 .
(4)E能转化为H.该反应的化学方程式为 .
(5)A、B、C、D、E、F、G、H 8种物质中能与盐酸反应的是 (写字母序号).
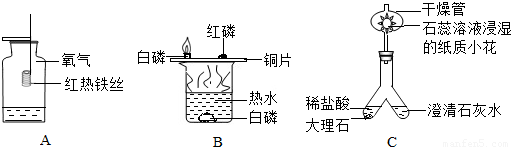
x气体可能由CH4、H2、CO中的一种或几种组成,某化学兴趣小组的同学利用如下装置进行实验验证该气体的组成.(碱石灰的主要成分为NaOH和CaO)

(1)写出CH4燃烧的化学反应方程式 .
(2)填写下列实验报告.
(3)若x气体燃烧后有水和二氧化碳生成,则x气体的组成可能为 .

(1)写出CH4燃烧的化学反应方程式 .
(2)填写下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 打开分液漏斗上端玻璃塞和下端活塞, | 若 | X气体为H2 |
| 若 | X气体为CO |
孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
查阅资料:①Cu2(OH)2CO3 2CuO+CO2↑+H2O 2CuO+C
2CuO+CO2↑+H2O 2CuO+C 2Cu+CO2↑
2Cu+CO2↑
②CuO为黑色固体,化学性质和氧化铁相似.
(1)实验l:加热分解碱式碳酸铜.装置如图所示.
①A中固体的变化为 .
②欲证明反应后有水生成,B中所盛试剂为 .
③反应结束时的操作应该是 ,理由是 .
(2)实验2:木炭和氧化铜反应.
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
做出猜想:剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜.
实验验证:填写下表.
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:
上述设计方案的主要研究方法是 .

0 79893 79901 79907 79911 79917 79919 79923 79929 79931 79937 79943 79947 79949 79953 79959 79961 79967 79971 79973 79977 79979 79983 79985 79987 79988 79989 79991 79992 79993 79995 79997 80001 80003 80007 80009 80013 80019 80021 80027 80031 80033 80037 80043 80049 80051 80057 80061 80063 80069 80073 80079 80087 211419
查阅资料:①Cu2(OH)2CO3
 2CuO+CO2↑+H2O 2CuO+C
2CuO+CO2↑+H2O 2CuO+C 2Cu+CO2↑
2Cu+CO2↑②CuO为黑色固体,化学性质和氧化铁相似.
(1)实验l:加热分解碱式碳酸铜.装置如图所示.
①A中固体的变化为 .
②欲证明反应后有水生成,B中所盛试剂为 .
③反应结束时的操作应该是 ,理由是 .
(2)实验2:木炭和氧化铜反应.
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
做出猜想:剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜.
实验验证:填写下表.
| 实验操作及现象 | 实验结论 |
| 该黑色粉末为氧化铜 |
| 配方l | 配方2 | 配方3 | 配方4 | |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |