题目内容
工业生产的纯碱产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取12g样品放在烧杯中并滴入稀盐酸.当稀盐酸滴加至71g时,恰好完全反应,烧杯内溶液的总质量为78.6g(假设产生的气体全部逸出).请计算:(1)生成CO2的质量为 .
(2)样品中碳酸钠的质量分数.
(3)若将所得溶液配制成10%的NaCl溶液需要加水的质量.
【答案】分析:根据化学方程式找出碳酸钠与氯化钠、二氧化碳的质量比;根据质量守恒定律结合由烧杯中物质的质量反应前后的变化可得出生成的二氧化碳的质量,然后根据化学方程式即可求出碳酸钠和生成的氯化钠的质量,然后求解(2)(3)题.
解答:解:(1)根据质量守恒定律,生成气体的质量为:71g+12g-78.6g=4.4g,故生成气体质量为4.4g
(2)解:设样品中碳酸钠的质量为x,生成NaCl质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
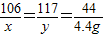
x=10.6g
y=11.7g
样品中碳酸钠的质量分数为: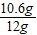 ×100%=88.3%
×100%=88.3%
答:样品中碳酸钠的质量分数为88.3%.
(3)设需要加水的质量为z
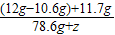 ×100%=10%
×100%=10%
z=52.4g
答:需要加水的质量为52.4g.
点评:本题主要考查化学方程式的书写、质量守恒定律和有关化学方程式的计算,只要看清反应前后烧杯中物质减轻是因为生成了气体二氧化碳即可顺利解答;计算是要细心、准确.
解答:解:(1)根据质量守恒定律,生成气体的质量为:71g+12g-78.6g=4.4g,故生成气体质量为4.4g
(2)解:设样品中碳酸钠的质量为x,生成NaCl质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
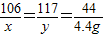
x=10.6g
y=11.7g
样品中碳酸钠的质量分数为:
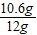 ×100%=88.3%
×100%=88.3%答:样品中碳酸钠的质量分数为88.3%.
(3)设需要加水的质量为z
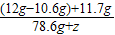 ×100%=10%
×100%=10%z=52.4g
答:需要加水的质量为52.4g.
点评:本题主要考查化学方程式的书写、质量守恒定律和有关化学方程式的计算,只要看清反应前后烧杯中物质减轻是因为生成了气体二氧化碳即可顺利解答;计算是要细心、准确.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是 .
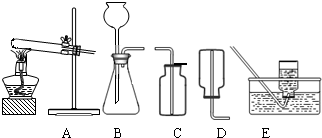
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为 ,制取和收集氨气可用下图中的 和 装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)