下表是氯化钠和硝酸钾的溶解度(部分):
(1)若要将接近饱和的硝酸钾溶液变为饱和溶液,可采取的方法有:①继续加入硝酸钾固体、② 、③ ;
(2)从结晶的方法看,海水晒盐属于 结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响 (选填“小”或“大”);
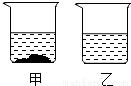
(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是 ,加入的质量范围为: .
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
| NaCl的溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 |
(2)从结晶的方法看,海水晒盐属于 结晶(选填“蒸发”或“降温”),使用该方法的原因是:氯化钠的溶解度受温度影响 (选填“小”或“大”);
(3)10℃时,在各盛有100g水的甲、乙两烧杯中,分别加入 等质量的氯化钠和硝酸钾固体,充分溶解后,现象如图所示.甲烧杯中加入的物质是 ,加入的质量范围为: .

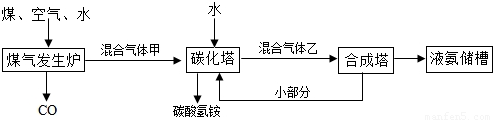
某同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色溶液(如右图所示),此溶液是什么?对此问题他进行了如下探究.
【猜想与假设】
猜想1:碳酸溶液 猜想2:过氧化氢溶液 猜想3:稀硫酸
【实验与结论】
【解释与讨论】
(1)实验②中反应的化学方程式为: ;
(2)为避免出现标签残缺的情况,在倾倒液体时应注意 ;
(3)若用100g 20%的过氧化氢溶液配制5%的稀溶液,稀释时要加水 毫升.

【猜想与假设】
猜想1:碳酸溶液 猜想2:过氧化氢溶液 猜想3:稀硫酸
【实验与结论】
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量该无色液体于试管中,加入 ,并加热 | 若 ,且加热无气泡产生 | 猜想1不正确. |
| ② | 向盛有少量二氧化锰的试管中加入适量的该无色液体,并将带火星的木条放在试管口 | 若试管内有大量气泡产生,且带火星的木条复燃 | 猜想2正确. |
| ③ | 向装有锌粒的试管中加入适量该无色液体,并将燃着的木条放在试管口 | 若管口没有火焰,也听不到“噗”的声音 | 猜想3 . |
(1)实验②中反应的化学方程式为: ;
(2)为避免出现标签残缺的情况,在倾倒液体时应注意 ;
(3)若用100g 20%的过氧化氢溶液配制5%的稀溶液,稀释时要加水 毫升.

下表提供了在一定条件下,水能否与一些金属发生反应的信息.
(1)铁在常温下与水不反应,但铁制品在潮湿的环境中容易生锈.铁锈主要成份的化学式是 ,它是一种 、多孔的物质.
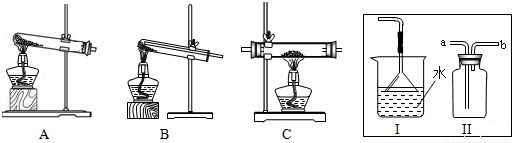
(2)某同学进行了如图所示实验,一周以后发现铁钉表面都锈蚀了.根据铁生锈的条件判断,图中a、b、c三处锈蚀情况最严重的是 (选填字母),比较b处与c处生锈程度可推测,影响铁生锈程度的因素是 .
(3)根据表中信息推断,镁与水蒸气 反应(选填“能”或“不能”).

| 物质 | 钠与冷水 | 镁与冷水 | 镁与水蒸气 | 铁与冷水 | 铁与水蒸气 |
| 能否发 生反应 | 剧烈反应 | 缓慢反应 | 加热条件下 反应 | 不反应 | 加热条件 下能反应 |
(2)某同学进行了如图所示实验,一周以后发现铁钉表面都锈蚀了.根据铁生锈的条件判断,图中a、b、c三处锈蚀情况最严重的是 (选填字母),比较b处与c处生锈程度可推测,影响铁生锈程度的因素是 .
(3)根据表中信息推断,镁与水蒸气 反应(选填“能”或“不能”).

已知CO与Fe2O3作用生成Fe的反应是分步进行的,反应中铁的氧化物中氧元素质量分数逐渐降低.
(1)上述三个反应发生的先后顺序是 .
(2)某同学取2.4g纯净的Fe2O3与CO反应一段时间后,对剩余固体的成分展开探究.
【实验过程】
【分析与结论】
小明认为该黑色粉末中一定含有铁;小军认为还需要再设计一个实验才能证明产物中含有铁,他的理由是 ;
小军设计的实验可能是(写出方法与现象) ;
【拓展延伸】
化学生产中往往会以某一种元素的转化来计算“反应的转化率”,其公式如下:
反应转化率= ;若以原固体中氧元素的转化来表达反应的转化率则该反应转化率为 .(结果用百分数表示,保留一位小数).
;若以原固体中氧元素的转化来表达反应的转化率则该反应转化率为 .(结果用百分数表示,保留一位小数).
0 68780 68788 68794 68798 68804 68806 68810 68816 68818 68824 68830 68834 68836 68840 68846 68848 68854 68858 68860 68864 68866 68870 68872 68874 68875 68876 68878 68879 68880 68882 68884 68888 68890 68894 68896 68900 68906 68908 68914 68918 68920 68924 68930 68936 68938 68944 68948 68950 68956 68960 68966 68974 211419
| 序号 | 化学反应 |
| ① | Fe3O4+CO FeO+CO2 FeO+CO2 |
| ② | 3Fe2O3+CO 2Fe3O4+CO2 2Fe3O4+CO2 |
| ③ | FeO+CO Fe+CO2 Fe+CO2 |
(2)某同学取2.4g纯净的Fe2O3与CO反应一段时间后,对剩余固体的成分展开探究.
【实验过程】
| 实验内容 | 实验现象 | |
| 实验一 | 冷却后,称量剩余固体 | 剩余固体质量为1.76g |
| 实验二 | 取一部分剩余固体,用磁铁靠近 | 部分粉末能被磁铁吸引 |
小明认为该黑色粉末中一定含有铁;小军认为还需要再设计一个实验才能证明产物中含有铁,他的理由是 ;
小军设计的实验可能是(写出方法与现象) ;
【拓展延伸】
化学生产中往往会以某一种元素的转化来计算“反应的转化率”,其公式如下:
反应转化率=
 ;若以原固体中氧元素的转化来表达反应的转化率则该反应转化率为 .(结果用百分数表示,保留一位小数).
;若以原固体中氧元素的转化来表达反应的转化率则该反应转化率为 .(结果用百分数表示,保留一位小数). 
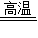 CO+H2,
CO+H2, 2NH3
2NH3