(5分)普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件。为测定黄铜中铜的质量分数,取样品10 g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)该过程中发生反应的化学方程式为 。
(2)黄铜中铜的质量分数为 。
(3)加入的稀硫酸溶液中硫酸的质量分数是 。(写出计算过程)
某校兴趣小组在实验室中完成制取氧气的实验,他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
1.完全反应后,生成氧气质量为 g;
2.原混合物中氯酸钾的质量分数是多少?(精确到0.1%)
3.试画出固体物质的质量(纵坐标)随反应时间(横坐标)的变化关系图.
给29.4克氯酸钾和二氧化锰的混合物加热,测得剩余固体的质量(m)与反应时间(t)的关系如下表:
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 29.4 | 27.4 | 25.4 | 23. 4 | 21.4 | 19.8 | 19. 8 |
(1)当氯酸钾完全反应后,生成氧气的质量为 g。
(2)剩余固体由哪些物质组成?它们的质量各为多少克?
某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:
Ⅰ.取一个三通管(三个管口都未密封,与空气相通),在三通管的上部和下部各放一张湿润的蓝色石蕊试纸(湿润的蓝色石蕊试纸遇到酸性物质会变红)。然后将它与二氧化碳的发生装置连接。(如图1,整套装置的气密性良好)
Ⅱ.打开分液漏斗的活塞,使石灰石与稀盐酸接触,观察到相关现象后,停止实验。
Ⅲ.取下图1中的三通管,把贴有试纸B的那端放在酒精灯火焰上加热(如图2),
观察实验现象。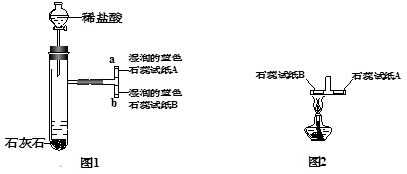
注:整个实验中不考虑反应过程中水分和HCl气体的挥发,且图1中产生的气流较缓慢
根据上述实验,回答下列问题:
(1)实验Ⅱ步骤中三通管内产生的实验现象是 __;由此说明二氧化碳气体具有 、 的性质。
(2)实验Ⅲ步骤中一定发生的化学反应方程式是 __;
(3)若不改变图1的实验装置,还要验证二氧化碳气体具有不能燃烧、也不能支持燃烧的性质,需要补充的实验是 __。
(4)取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应。有关实验数据如下表:(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,且不考虑反应过程中水分和HCl气体的挥发)
| | 反应前 | 反应后 | |
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
②该石灰石样品中碳酸钙的质量分数为 __(结果精确到0.1%)。
(8分)某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分数为10%的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0 g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.3g | 0.3g |
(1)2.0g石灰石样品中碳酸钙的质量为 ,石灰石中碳酸钙的质量分数为 。
(2)请你继续计算反应生成溶液中氯化钙的质量分数(计算过程和结果均保留一位小数)。
(3分)甲、乙两种分子的结构示意图如下。“○”和“ ”分别表示氢和氧两种元素的原子。(已知氢、氧两种原子的相对原子质量分别为:H-1 O-16)
”分别表示氢和氧两种元素的原子。(已知氢、氧两种原子的相对原子质量分别为:H-1 O-16)
| 分子 | 甲 | 乙 |
| 结构示意图 |  | 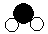 |
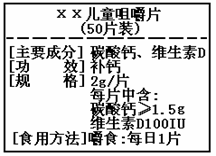
 Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。
Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。