氯化钠和碳酸钠晶体的溶解度(0℃~30℃)如下表所示:
(1)根据上表分析,碳酸钠晶体的溶解度随温度 .
(2)将含水各100g的氯化钠与碳酸钠的饱和溶液,从30℃降至0℃时,析出氯化钠晶体的质量 (填“大于”“小于”或“等于”)碳酸钠晶体的质量.
(3)欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取 方法.
(4)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是 .
A、①所得溶液中溶质质量分数为20% B、②中所得溶液是不饱和溶液
C、20℃时10g水最多能溶解4g NaCl D、③④溶液中溶质质量分数相等.
0 31888 31896 31902 31906 31912 31914 31918 31924 31926 31932 31938 31942 31944 31948 31954 31956 31962 31966 31968 31972 31974 31978 31980 31982 31983 31984 31986 31987 31988 31990 31992 31996 31998 32002 32004 32008 32014 32016 32022 32026 32028 32032 32038 32044 32046 32052 32056 32058 32064 32068 32074 32082 211419
| 0℃ | 10℃ | 20℃ | 30℃ | |
| NaCl(g) | 35.7 | 35.8 | 36.0 | 36.3 |
| Na2CO3晶体(g) | 7.0 | 12.5 | 21.5 | 38.8 |
(2)将含水各100g的氯化钠与碳酸钠的饱和溶液,从30℃降至0℃时,析出氯化钠晶体的质量
(3)欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取
(4)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是
| 实验序号 | 水的质量(g) | 加入NaCl的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
C、20℃时10g水最多能溶解4g NaCl D、③④溶液中溶质质量分数相等.
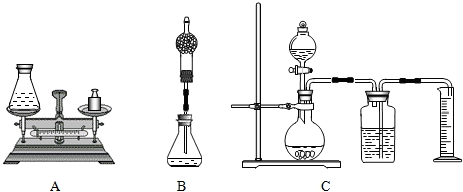


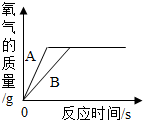 化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空: 26、食醋、食盐、碱面、蔗糖、花生油、大米、矿泉水都是厨房常备物品.
26、食醋、食盐、碱面、蔗糖、花生油、大米、矿泉水都是厨房常备物品.