为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
(1)上述反应的化学方程式为 ;
(2)根据锌的质量列出求解第二次生成氢气质量(x)的比例式 ;
(3)所用稀盐酸中溶质的质量分数为 ;
(4)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为 ;
(5)黄铜样品中铜的质量分数为 .
0 31807 31815 31821 31825 31831 31833 31837 31843 31845 31851 31857 31861 31863 31867 31873 31875 31881 31885 31887 31891 31893 31897 31899 31901 31902 31903 31905 31906 31907 31909 31911 31915 31917 31921 31923 31927 31933 31935 31941 31945 31947 31951 31957 31963 31965 31971 31975 31977 31983 31987 31993 32001 211419
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
(2)根据锌的质量列出求解第二次生成氢气质量(x)的比例式
(3)所用稀盐酸中溶质的质量分数为
(4)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为
(5)黄铜样品中铜的质量分数为
 9、常温下氯气(Cl2)是一种黄绿色的气体,密度比空气大,可溶于水,有剧毒,能与水、碱等物质发生化学反应.若在实验室收集氯气,正确的装置是( )
9、常温下氯气(Cl2)是一种黄绿色的气体,密度比空气大,可溶于水,有剧毒,能与水、碱等物质发生化学反应.若在实验室收集氯气,正确的装置是( )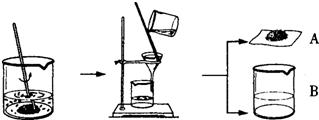
 23、用五个圆表示A(氧化铁)、B(稀硫酸)、C(碳酸钠溶液)、D(稀盐 酸)、E(氯化钡溶液)五种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题:
23、用五个圆表示A(氧化铁)、B(稀硫酸)、C(碳酸钠溶液)、D(稀盐 酸)、E(氯化钡溶液)五种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题: 22、水是一种宝贵的自然资源,当今世界淡水资源日趋紧张.如图是童童同学三月份为班级板报绘制的一幅画,
22、水是一种宝贵的自然资源,当今世界淡水资源日趋紧张.如图是童童同学三月份为班级板报绘制的一幅画,
 19、实验室现有大理石、高锰酸钾、稀盐酸、稀硫酸和紫色石蕊溶液及相关的仪器和用品,小辉同学要通过实验验证二氧化碳能与水反应的性质.请结合右图回答下列问题:
19、实验室现有大理石、高锰酸钾、稀盐酸、稀硫酸和紫色石蕊溶液及相关的仪器和用品,小辉同学要通过实验验证二氧化碳能与水反应的性质.请结合右图回答下列问题: