0 30448 30456 30462 30466 30472 30474 30478 30484 30486 30492 30498 30502 30504 30508 30514 30516 30522 30526 30528 30532 30534 30538 30540 30542 30543 30544 30546 30547 30548 30550 30552 30556 30558 30562 30564 30568 30574 30576 30582 30586 30588 30592 30598 30604 30606 30612 30616 30618 30624 30628 30634 30642 211419

 ,推测下列元素的单质与金属钠的化学性质相似的是( )
,推测下列元素的单质与金属钠的化学性质相似的是( )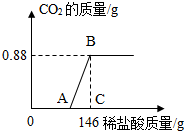 某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解)
某兴趣小组同学对于实验室制得的烧碱粗产品(杂质为Na2CO3和NaCl)进行了测定分析.取20.0g烧碱粗产品,逐滴滴入10%的盐酸至过量,消耗的稀盐酸与生成CO2的质量关系如下图所示(不考虑二氧化碳气体的溶解) 一双善于发现惘题的眼睛能够带来许多意想不到的知识.
一双善于发现惘题的眼睛能够带来许多意想不到的知识.