题目内容
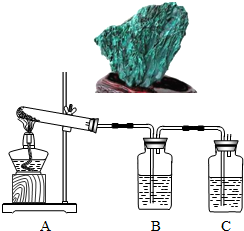
如图所示,某校同学进行的金属铜冶炼原理的探究,请完成下列填空.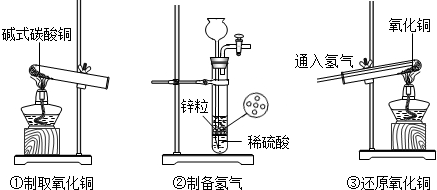
查阅资料:Cu2(OH)2CO3受热易分解生成氧化铜和水同时放出二:氧化碳,氢气可以还原氧化铜得到金属铜.
(1)实验①中判断碱式碳酸铜已经完全分解的依据是
(2)实验②制备氢气时,应如何检验气密性
(3)制备的氢气必须检验纯度,还原氧化铜时必须通入氢气一段时间后才能加热,目的都是为了
| ||
(2)检查装置气密性可以利用加水形成液柱的不变进行,所以本题答案为:关闭活塞,从长颈漏斗向试管内倒水至浸没漏斗末端,继续加水,会在漏斗颈形成液柱;
(3)氢气是可燃性气体,不纯时加热或点燃会引起爆炸,氢气与氧化铜反应能生成铜和水,反应后继续通入氢气能防止生成的铜重新被氧化,所以本题答案为:防止爆炸,
H2+CuO
| ||

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
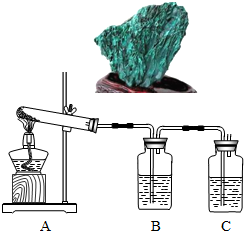
名校名卷单元同步训练测试题系列答案(7分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料。某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理。
【查阅资料】
1.Cu2(OH)2CO3  2CuO+CO2 + H2O
2CuO+CO2 + H2O
2CuO+C 2Cu + CO2 ↑
2Cu + CO2 ↑
2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。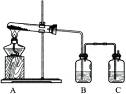
①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
| 实验操作及现象 | 实验结论 |
| | 该黑色粉末为氧化铜 |
| | 配方l | 配方2 | 配方3 | 配方4 |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
(7分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料。某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理。

【查阅资料】
1.Cu2(OH)2CO3
 2CuO+CO2 + H2O
2CuO+CO2 + H2O
2CuO+C 2Cu
+ CO2 ↑
2Cu
+ CO2 ↑
2.CuO为黑色固体,化学性质和氧化铁相似。
(1)实验l:加热分解碱式碳酸铜。装置如图所示。
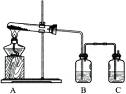
①A中固体的变化为____。
②欲证明反应后有水生成,B中所盛试剂为____。
③反应结束时的操作应该是____,理由是____。
(2)实验2:木炭和氧化铜反应。
将木炭粉末和氧化铜粉末混合均匀,放进试管加热,反应后将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余。该小组同学设计方案验证黑色粉末的成分。
【作出猜想】
剩余黑色粉末可能是:①氧化铜;②木炭;③木炭和氧化铜。
【实验验证】填写下表。
|
实验操作及现象 |
实验结论 |
|
|
该黑色粉末为氧化铜 |
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比,设计方案如下:
|
|
配方l |
配方2 |
配方3 |
配方4 |
|
木炭质量(g) |
0.4 |
0.5 |
0.6 |
0.7 |
|
氧化铜质量(g) |
8 |
8 |
8 |
8 |
上述设计方案的主要研究方法是__________________。
 (2012?大兴区二模)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.
(2012?大兴区二模)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],绿色并具有浓淡的条状花纹(见右图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.某校课外小组同学欲在实验室验证碱式碳酸铜制铜的反应原理.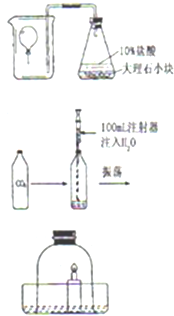 在学习完二氧化碳的性质以后,某校化学小组的同学们设计了下列趣味实验,如图所示,请结合实验回答下列问题
在学习完二氧化碳的性质以后,某校化学小组的同学们设计了下列趣味实验,如图所示,请结合实验回答下列问题