在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法正确的是________
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 3 | 90 | 0 |
| 反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
B.Y一定是催化剂
C.该反应是分解反应
D.________.
下列说法不正确的是
- A.生活中可用加热煮沸的方法降低水的硬度
- B.公交车上的“CNG”标志是代表其燃料为压缩天然气
- C.当试管口径较大时,可用药匙将溶液送入试管中
- D.氢氧化钠有腐蚀性,应该放入玻璃器皿中称量
 硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
Ⅰ、硫酸铜的制备
(1)某学习小组同学利用铜屑、稀硫酸为原料制备硫酸铜.其原理是在高温条件下将铜粉反复灼烧,使铜充分氧化成氧化铜,再将氧化铜与稀硫酸反应制备硫酸铜,请写出相应的化学方程式________、________;
(2)通过查阅资料,同学们找到了一种工业制备硫酸铜晶体(CuSO4?xH2O)的流程,具体如下:将铜丝放到稀硫酸中,控温在50℃.加入10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发、降温结晶等,用少量95%的酒精淋洗后晾干,得CuSO4?5H2O.
①写出该工艺流程生成CuSO4的化学方程式________;
②在上述生产过程中,控制温度在50℃和60℃加热的原因为________,
③上述生产流程的优点有________(写出一种即可);
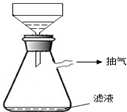
④在过滤时,采用了右图所示的装置,你认为这样做的优点是________;
Ⅱ、硫酸铜的应用及相关实验
(1)波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu4(OH)6SO4,其中铜元素的化合价为________,该化学式可以写成盐和碱的形式________,其杀菌机理可看作是Cu2+使病原菌失去活性,这说明病原菌的主体是________(填一种有机物名称).
(2)为验证Al的化学性质比铜活泼,小怡做了以下实验,现象如下表:
| Al片(未打磨) | Al片(打磨) | |
| CuSO4溶液 (5%,5mL) | 无变化,数小时后铝片上附有极少气泡,几乎无红色物质 | 极少气泡,附着极少红色物质,持续较长时间 |
| CuSO4溶液 (10%,5mL) | 无变化,数小时后铝片附有稍多气泡,仅有极少红色斑点 | 稍多气泡,附着极少(多于5%)红色物质,持续较长时间 |
| CuCl2溶液 (5%,5mL) | 多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高 | 更多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高 |
①铝和铜盐溶液反应速率与________、________和________有关,同时说明铜盐溶液中的Cl-能________(填“加快”或“抑制”)反应速率,若实验室没有CuCl2溶液,则可以在CuSO4溶液中加入少许________(填物质名称),以使实验现象更为明显;
②该反应过程要________(填“吸热”或“放热”).经检验,产生的气体是一种能燃烧的单质,该气体是________(填化学式);
Ⅲ、硫酸铜晶体(CuSO4?xH2O)中结晶水(xH2O)含量的测定
在老师的指导下,学习小组取12.5g硫酸铜晶体(CuSO4?xH2O)进行热分解,获得相关数据,并绘制成固体质量-温度的关系如下图.
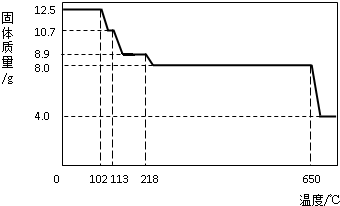
(1)在加热过程中,随着水分的蒸发,固体颜色将由蓝色逐渐变为________色,最终变为黑色;
(2)写出固体质量由10.7g变为8.9g时的化学方程式________;
(3)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为________;
(4)根据图中数据,计算CuSO4?xH2O中的CuSO4的质量分数.(要求:根据x的值进行计算,CuSO4的相对分子质量:160,H2O的相对分子质量:18)