我国青海湖采集的天然碱样品可表示为aNa2CO3?bNaHCO3?cH2O(a、b、c为最简整数比).小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
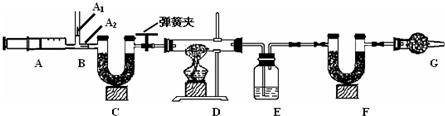
已知:1、碳酸钠比较稳定,加热时不分解;
2、2NaHCO3
Na2CO3↑+CO2↑+H2O
3、图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
(1)E中的药品为 ,E的作用是 .
C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是
,F的作用是 ,G的作用是 .
(2)实验步骤②与③能否颠倒 (填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是
(3)据右表数据计算可得:天然碱的化学式中a:b:c= .

已知:1、碳酸钠比较稳定,加热时不分解;
2、2NaHCO3
| ||
3、图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
(1)E中的药品为
C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是
(2)实验步骤②与③能否颠倒
(3)据右表数据计算可得:天然碱的化学式中a:b:c=
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
22、举例来证明下列结论是错误的:
(1)金属都能和酸发生置换反应生成盐和氢气
(2)生成沉淀的反应一定是复分解反应
(3)物质的溶解度随着温度的升高都会增大
(1)金属都能和酸发生置换反应生成盐和氢气
铜与盐酸
.(2)生成沉淀的反应一定是复分解反应
二氧化碳和石灰水反应
.(3)物质的溶解度随着温度的升高都会增大
氢氧化钙或气体
. 29、小刚为了解生活中常见的锌锰干电池,做了以下探究:他打开一节废电池,观察到如下现象:①黑色碳棒完好无损;②电极周围充满黑色粉末;③里面有少量无色晶体;④金属外壳明显破损.
29、小刚为了解生活中常见的锌锰干电池,做了以下探究:他打开一节废电池,观察到如下现象:①黑色碳棒完好无损;②电极周围充满黑色粉末;③里面有少量无色晶体;④金属外壳明显破损.