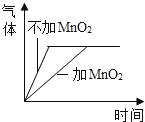
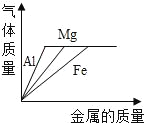
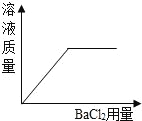
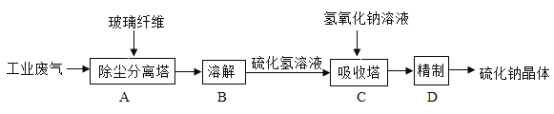
【题目】常见金属在氧气中能剧烈燃烧。某化学探究小组对“铁丝在氧气中燃烧为什么会火星四射”有兴趣。于是进行了如下探究:
(提出问题)铁丝在氧气中燃烧会火星四射与哪些因素有关呢?
(猜想与假设)猜想一:可能与金属的沸点有关;猜想二:可能与氧气的浓度有关;猜想三:可能与铁中含碳量有关。
(查阅资料)镁的沸点为1107℃;铁的沸点为2705℃。
(设计并实验)该探究小组用将镁丝、纯细铁丝和两种不同含碳量的细铁丝(镁丝和铁丝直径均为0.4mm)分别放入空气和氧气中燃烧。记录燃烧时的现象如下表。
实验序号 | 氧气纯度(含氧量) | 镁丝 | 铁丝中含碳量 | 燃烧时的现象 |
① | 空气中(21%) | 剧烈燃烧,发出耀眼白光,无火星 | 0%(纯铁) | 不燃烧 |
② | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0%(纯铁) | 剧烈燃烧,无火星 |
③ | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0.05% | 剧烈燃烧,极少火星 |
④ | 纯氧中(100%) | 更剧烈燃烧,发出耀眼白光,无火星 | 0.6% | 剧烈燃烧,火星四射 |
(收集证据)(1)若要比较细铁丝燃烧的剧烈程度与氧气的纯度有关,应选择的实验编号组合是_____。由实验③和④对比可知,产生火星四射的现象与细铁丝中含碳量的关系:_____。
(解释与结论)(2)通过探究,了解细铁丝在纯净的氧气燃烧时会火星四射的原因。请写出细铁丝在氧气中燃烧生成黑色的四氧化三铁固体的化学方程式为:_____。
(3)细铁丝中含有不同的含碳量,碳元素在燃烧过程中生成二氧化碳气体,将反应生成的熔化物四氧化三铁推了出去,从而产生了火星四射的现象。为保证实验成功,选用的铁丝中含碳量要控制的范围为_____。
(4)取一段含碳量0.6%的细铁丝绕成螺旋状,投入盛有足量的稀盐酸的烧杯中充分反应,可观察的现象为_____,并在烧杯底有少量的黑色残渣,其化学式为C。
【题目】某兴趣小组同学为了探究木炭与氧化铜反应得到的红色固体的成分,进行了如下探究活动:
探究一:木炭与氧化铜反应生成红色固体的原因是什么?
(1)设计如图装置并实验,加热一段时间后,可发现右侧的试管中的澄清石灰水中的现象是_____,左侧试管中黑色粉末变成红色,由此得出:木炭具有的化学性质为_____。

(2)这套装置使用酒精喷灯加热,也可在酒精灯上加网罩,其目的是_____。
探究二:木炭与氧化铜反应得到的红色固体是什么?
(查阅资料)(3)氧化亚铜(Cu2O)是一种红色固体,可用于船底防污漆,用于防止海生物对船舶设备的污损。氧化亚铜能与稀硫酸发生反应:Cu2O+H2SO4=CuSO4+X+H2O,则X的化学式为_____。
(进行实验)限选试剂:稀硫酸;仪器:试管、玻璃棒、漏斗、铁架台、烧杯。
实验步骤及操作 | 实验现象 |
步骤I:取充分反应后生成的少量红色固体,加入到足量硫酸溶液中,观察现象。 步骤II:将充分反应后的溶液过滤。 | a.过滤后有红色固体; b.溶液呈蓝色。 |
(4)观察到的实验现象说明了木炭与氧化铜充分反应后所得到的红色固体中一定含有氧化亚铜,_____(填“一定”或“不一定”)还含有铜。木炭与氧化铜在高温下生成氧化亚铜和二氧化碳,该反应的化学方程式为:_____。
【题目】经实验测定氯化钠和硝酸钾在不同温度的溶解度数据如下表。下列说法不正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
NaCl/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
KNO3/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
A.KNO3 和NaCl的溶解度相等的温度在20℃~30℃之间
B.两种物质的溶解度都随温度的升高而增大
C.在20℃时,10g水中加入5gNaCl可得到质量分数为33.3%的NaCl溶液
D.分别将两种物质的100g饱和溶液从50℃降至10℃,KNO3析出的晶体多