【题目】某研究小组对过氧化氢溶液制取氧气进行如下探究。
实验一 氧气制取实验
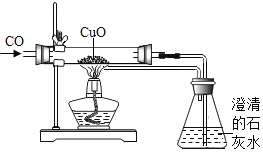
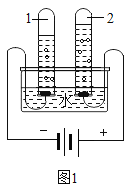
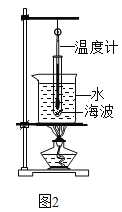
(1)现有如下装置:

①仪器a的名称是____________。
②实验室用过氧化氢溶液制氧气,应选择的发生装置是_____________(填字母), 反应的的文字(符号)表达式为_____________。如果选用D收集氧气,依据的原理是____________,验满的方法是____________。
③选用C装置收集气体时,下列实验操作正确的是____________ (填序号, 可多选)。
A 反应前,将集气瓶住满水,用玻璃片盖着瓶口,倒立在盛水的水糟中
B 导管口开始有气泡放出时,立即将导管口移入集气瓶
C 收集气体后,将集气瓶盖上玻璃片再移出水槽
实验二探究H2O2质量分数、溶液pH、温度对反应速率的影响
资料:溶液pH表示溶液的酸碱度,即所含氢离子浓度的负对数,氢离子浓度越大,pH越小。
(2)设计如下表实验方案:
实验序号 | H2O2质量分数% | pH | 温度/°C | 每分钟气泡数 |
1 | 30 | 5 | 20 | |
2 | 30 | 6 | 20 | |
3 | 30 | 11 | 20 | |
4 | 15 | 11 | 30 | |
5 | a | 11 | b |
①实验1~3的实验目的是____________________________。
②a=______________;b=_____________。
实验三探究制取氧气的适宜催化剂
(3)实验方案如下:
Ⅰ用MnO2、CuO、 Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ取30粒含MnO2的海藻酸钠微球,采用左下图装置进行实验。改用其他三种微球,分别重复上述实验,得到图的锥形瓶内压强随时间变化的曲线图。

①每次实验时,海藻酸钠微球数应相同的原因是________________。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_________________。
③从实验曲线看,催化效果较好、反应温和的催化剂是__________________。
【题目】阅读下面科普短文,回答问题。
美食伴侣·味精

味精,是国内外广泛使用的增鲜调味品之一,为白色柱状结晶体,其主要成分为谷氨酸钠(C5H8NO4Na)和食盐。味精被摄入人体中,谷氨酸钠与胃酸作用生成谷氨酸和氯化钠,很快被消化吸收为蛋白质,并参与人体中的多种新陈代谢。味精的使用浓度占食品重量的0.2% ~ 0.8%能最大程度增进食品的天然风味。味精的鲜味受什么因素影响呢?经实验测定发现,当加热至100℃以上时,会引起部分失水,生成焦谷氨酸钠,失去鲜味,且有轻微毒性。下表是焦谷氨酸钠含量与加热温度、加热时间的关系。
加热时间(小时)] | 焦谷氨酸钠含量(%) | ||
100℃ | 107℃ | 115℃ | |
0.5 | 0.3 | 0.4 | 0.7 |
1.0 | 0.6 | 0.9 | 1.4 |
2.0 | 1.1 | 1.9 | 2.8 |
4.0 | 2.1 | 3.6 | 5.7 |
实验研究还表明,味精对婴幼儿,特别是几周以内的婴儿生长发育有严重影响。它能使婴幼儿血中的锌转变为谷氨酸锌随尿排出,造成体内缺锌,影响宝宝生长发育,并产生智力减退和厌食等不良后果。因此产后3个月内乳母和婴幼儿的菜肴不要加入味精。请根据文章内容回答下列问题:
(1)谷氨酸钠的物理性质有____________________________。
(2)谷氨酸钠进入人体后会转化为_______________________。
(3)谷氨酸钠(C5H8NO4Na)中碳、氢元素的质量比为_____________。
(4)写出谷氨酸钠与胃酸作用生成物之一的氯化钠的化学式为__________。
(5)下列关于味精的说法中,合理的是_________(填序号)。
A. 炒菜时加入味精后生成焦谷氨酸钠的含量只与加热时间有关
B. 烹饪时加入味精的最佳时间是大火翻炒时
C. 婴幼儿的食品中不应该加入味精
【题目】某化学兴趣小组对氯酸钾制取氧气的催化剂展开探究。请回答下列问题:
探究一:二氧化锰粒径大小对催化效果的影响

取两份等质量氯酸钾,分别加入等质量、粒径大小不同的二氧化锰进行加热,用传感器测得固体残留率(反应后剩余固体质量与反应前固体质量之比)如右图:
(1)二氧化锰作催化剂,加热氯酸钾制取氧气的化学方程式为_____________。
(2)查阅资料得知,发生反应的温度越低,催化效果越好。分析上图,对氯酸钾分解催化效果更好的是_____________。催化效果更好的原因可能是_____________。
探究二:催化剂用量及催化剂种类对催化效果的影响
同学们设计如下实验方案:
编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集VmL氧气 所需时间/s |
实验1 | 5 | 171 | ||
实验2 | 5 | 二氧化锰 | 0.25 | 79 |
实验3 | 5 | 二氧化锰 | 0.5 | 49 |
实验4 | 5 | 二氧化锰 | 2.5 | 93 |
实验5 | 5 | 氧化铁 | 0.5 | 58 |
实验6 | 5 | 氯化钾 | 0.5 | 154 |
(3)表中所列三种催化剂中,催化效果最好的是_____________。
(4)二氧化锰与氯酸钾的质量比为_____________时,催化效果最好。
(5)氯化钾_____________(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集VmL氧气,所需时间明显少于171s,原因是_____________。
探究三:二氧化锰质量在反应前后的变化
同学们发现每次用氯酸钾和二氧化锰制取氧气结束后,在拆卸装置时总能闻到刺激性气味。他们将加热后剩余固体中的二氧化锰分离并测量其质量,发现总小于加热前二氧化锰的质量。查阅资料后发现,一般认为加热氯酸钾和二氧化锰混合物的反应过程如下:
第1步: ![]() (其中Cl2有刺激性气味)
(其中Cl2有刺激性气味)
第2步: ![]()
第3步: ![]()
(6)第3步反应中锰元素化合价变化为_____→________。
(7)反应后剩余固体中二氧化锰质量小于反应前的质量,原因可能是_____________。