【题目】学习金属化学性质时,小红同学对“锌与硫酸反应快慢的影响因素”进行了探究。锌与硫酸反应的化学方程式是_____。
(提出问题)锌与硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
(设计并实验)小红用不同质量分数的硫酸和不同形状的锌进行下表所示实验。
实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积/mL(均集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(收集证据)
(1)比较不同形状的锌对反应快慢的影响,选拌的实验编号是_____。
(2)比较不同质量分数的硫酸对反应快慢的影响,选择的实验编号是_____。
(得出结论)结论是①_____;②_____。
(评价与反思)
(l)下表是小组同学第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 6.0mL |
第2分钟以后反应变慢是因为______________。
(2)实验结束发现实验用的试管内有白色晶体,显然不是剩余的锌,它应该是_____,产生这些白色晶体的原因是_____。
【题目】某同学用如下装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去)。
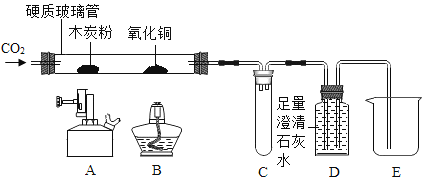
在完成气密性检查后加入药品,并已设法在玻璃管中充满二氧化碳。
实验步骤 | 实验现象 | 实验分析 |
①缓缓通入CO,点燃A处酒精喷灯,一段时间 | 木炭粉减少,D中有气泡、石灰水变浑浊且_____ | 玻璃管中反应的化学方程式_____,D中反应的化学方程式_____ |
②接下来点燃B处酒精灯,一段时间 | B处玻璃管内_____ | 实验说明_____具有还原性 |
③夹上弹簧夹停止通CO2,熄灭A、B火焰 | C中_____ | / |
有同学认为该装置需要添加尾气处理装置,你认为是否需要并说明理由_____。
【题目】溶液在生命活动和生产、生活中都起到十分重要的作用,
(1)食盐、蔗糖、花生油分别加入水中,不能形成溶液的是_____。
(2)t℃时向质量均为50g的4份水中分别加入一定量的KNO3固体,充分搅拌。加入KNO3的质量与所得溶液的质量如下表:
实验编号 | a | b | c | d |
加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
所得溶液的质量 | 95 | 100 | 105 | 105 |
①实验a、b、c、d中,有未被溶解的KNO3固体的实验是_____(填写实验编号)。
②t℃时KNO3的溶解度是_____.
③实验所得溶液中质量分数大小关系为:a<b_____c_____d.
④不改变温度,把实验b所得溶液变为质量分数20%,可以采取的操作是_____
(3)向一定量澄清的石灰水中加入少量生石灰,溶液立即变浑浊,可能的原因是_____
A 原石灰水已经饱和,生石灰与水反应的产物不能继续溶解
B 生石灰与水反应放热,溶液温度升高,溶质的溶解度降低
C 空气中的二氧化碳与石灰水反应生成了难溶物质
D 生石灰与水反应消耗了水,溶剂减少,有溶质析出