题目内容
【题目】人类的生活和生产都离不开金属材料。
(1)金属以矿物形式存在,下列矿石的主要成分属于氧化物的是_____(填序号)。
①赤铁矿(主要成分Fe2O3);②菱铁矿(主要成分FeCO3);③铝土矿(主要成分Al2O3)
(2)下列金属制品的用途中,利用金属延展性的是_____(填字母序号)。

(3)月饼中常见“双吸剂”,主要成分是铁粉。其防腐原理是_____.
(4)为了保护有限的金属资源,下列做法合理的是_____(填序号).
A 回收铝制饮料瓶
B 在铁制品表面涂油漆,防止生锈
C 尽量将已探明的铁矿全部开采
D 积极研发新材料以替代金属材料
(5)化学小组对含有硫酸铜和硫酸锌的废液进行了如下处理:
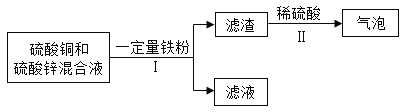
①步骤1中发生反应的化学方程式是_____,所属基本反类型是_____.步骤1的操作名称是_____。
②滤液中溶质有_____
【答案】①③ C 铁生锈消耗氧气和水 ABD Fe+CuSO4=FeSO4+Cu 置换反应 过滤 硫酸锌,硫酸亚铁
【解析】
(1)Fe2O3和 Al2O3属于氧化物,FeCO3不属于氧化物,故选①③;
(2)A、铁锅是利用铁的导热性;
B、铜导线是利用铜的导电性;
C、铝箔是利用铝的延展性;故选C;
(3)铁粉防腐的原理是铁生锈消耗氧气和水,防止食物变质;
(4)回收铝制饮料瓶、在铁制品表面涂油漆,防止生锈、积极研发新材料以替代金属材料都可以保护金属资源,而尽量将已探明的铁矿全部开采则不利于保护金属资源,故选ABD;
(5)①步骤1中铁和硫酸铜溶液反应生成硫酸亚铁和铜,反应的化学方程式是Fe+CuSO4=FeSO4+Cu;
该反应是铁将硫酸铜溶液中的铜置换出来,属于置换反应;
经过步骤1后得到滤渣和滤液,故步骤1的操作名称是过滤;
②滤液中含有未参与反应的硫酸锌以及反应生成的硫酸亚铁。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案