【题目】某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后。过滤,回收二氧化锰固体,并得到氯化钾溶液200g。
加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 26.0 | 23.4 | 16.4 | 16.4 |
(1)共制得氧气质量为_____。
(2)求理论上可回收二氧化锰的质量。_______
【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:不相等; 猜想2:相等。
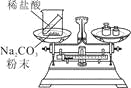
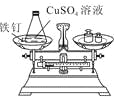
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲 组 | 乙 组 | |
实验 |
|
|
实验 | 有气泡产生, | 铁钉表面有红色物质析出, |
结论 | 猜想1正确 | 猜想2正确 |
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在 中进行。
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是 (填序号),从另外两种装置中任选一种指出其不足 。
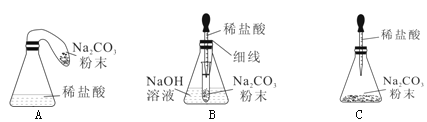
【得出结论】同学们利用改进后的最佳装置进行再次探究,均得出猜想二正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,
最终得出结论是: 的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由 种元素组成。