【题目】洁厕灵是常用的陶瓷清洗液,小彭同学对某品牌洁厕灵的有效成分及其含量进行研究。
(1)查阅资料得知:洁厕灵的有效成分是HCl,HCl的含量可通过已知溶质质量分数的NaHCO3溶液来测定,其他成分均不参与反应。请完成HCl与NaHCO3反应的化学方程式:HCl+NaHCO3=NaCl+___+CO2↑。
(2)向一锥形瓶中加入100 g该品牌的洁厕灵,再逐次加入相同质量分数的NaHCO3溶液,测出每次锥形瓶中反应后溶液的总质量,数据记录如下:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入NaHCO3溶液的质量/g | 40 | 40 | 40 | 40 | 40 |
反应后溶液的总质量/g | 138.9 | 177.8 | 216.7 | 255.6 | 295.6 |
① 第________次恰好完全反应。
② 该品牌洁厕灵中HCl的质量分数是多少?________
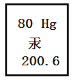
【题目】氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙![]() 遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的
遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的![]() 加入
加入![]() 溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
(提出问题)滤液中溶质的成分是什么?
猜想一:NaOH猜想二:NaOH、![]()
猜想三:NaOH、![]() 猜想四:NaOH、
猜想四:NaOH、![]() 、
、![]()
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因______。
(实验验证)
实验 | 现象 | 结论 |
| 无明显现象 | 猜想 ______ 不成立 |
| ______ | 猜想三成立 |
(反思与拓展)
![]() 写出氢化钙
写出氢化钙![]() 与水反应的化学方程式______。
与水反应的化学方程式______。
![]() 若向
若向![]() 的溶液中加入一定量的
的溶液中加入一定量的![]() ,充分反应,产生的气体有氢气和______。
,充分反应,产生的气体有氢气和______。
![]() 登山运动员携带
登山运动员携带![]() 作为能源提供剂与携带氢气相比,其优点是______
作为能源提供剂与携带氢气相比,其优点是______![]() 写一条即可
写一条即可![]() 。
。
【题目】结合下列过程,回答有关问题。
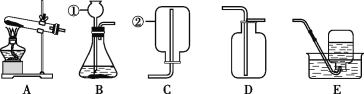
(1)写出标号仪器的名称:①____,②____。
(2)实验室制取并收集二氧化碳的装置组合为____,化学方程式为____。
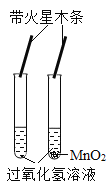
(3)写出实验室用高锰酸钾制取O2的化学方程式:______。试管口放一团棉花的目的是____,用E装置收集满时,接下来的操作顺序是____(填序号)。
①用玻璃片盖住集气瓶 ②将集气瓶正放在桌面 ③熄灭酒精灯 ④移出导管
(4)向5mL 5%的H2O2溶液中加入2滴一定浓度的FeCl3溶液,立即产生大量气泡。已知FeCl3溶液中主要含有三种微粒:H2O、Fe3+、Cl-。
[问题] 哪种微粒对H2O2溶液的分解起催化作用?
[假设] 假设一:可能是H2O;假设二:可能是Fe3+;假设三:可能是Cl-。
[分析] 假设一不可能成立,理由是______。
[实验]
操作 | 现象 | 结论 |
其他条件不变,向H2O2溶液中加入NaCl溶液 | 无明显变化 | 假设____成立 |
其他条件不变,向H2O2溶液中加入Na2SO4溶液 | 无明显变化 | |
其他条件不变,向H2O2溶液中加入Fe2(SO4)3溶液 | 立即产生大量气泡 |
(5)从循环利用的角度分析,二氧化锰与氯化铁溶液相比,____(填化学式)更适合作该反应的催化剂。