【题目】化学课上老师演示在氢氧化钠溶液中滴加稀盐酸实验时,出现了有气泡产生的现象,同学们计划对产生该现象的原因进行探究。
(提出问题)产生的气体成分是什么?
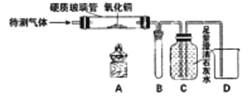
(设计实验)将生成的气体通入澄清的石灰水,石灰水变浑浊。
(分析与讨论)①生成的气体是_____。
②氢氧化钠已变质,变质的原因用化学方程式表示为_____。
(进一步探究)氢氧化钠溶液变质的程度如何?
(实验方案)
方案1:取少量氢氧化钠溶液的样品于一洁净试管中,先滴加酚酞溶液,酚酞变红色,再滴加氯化钙溶液,出现白色沉淀。
方案2:取少量氢氧化钠溶液的样品于一洁净试管中,先滴加澄清石灰水,出现白色沉淀,静置,再在上层溶液中滴加酚酞溶液,酚酞变红色。
(分析与讨论)同学们认为以上两个方案都不正确。
方案1不正确的原因是_____。
方案2不正确的原因是_____。
经过讨论同学设计了以下方案,得到了合理的结论。
实验步骤 | 实验现象 | 实验结论 |
(1)取少量氢氧化钠溶液的样品于一洁净试管中,先滴加过量的氯化钙溶液,观察现象。 | _____ | 氢氧化钠部分变质 |
(2)再向其中滴几滴酚酞溶液。 | 酚酞变红色。 |
实验中滴加过量氯化钙溶液的目的是_____。
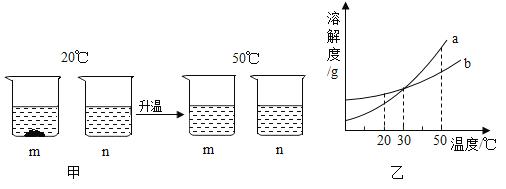
在氢氧化钠溶液中滴加稀盐酸,溶液温度与滴加稀盐酸质量之间的变化关系如图所示:
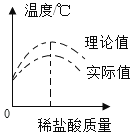
(1)实验中发现稀盐酸质量为m1时,测得的溶液温度最高,从能量的角度分析,氢氧化钠与稀盐酸的反应是_____反应;从反应进行的程度分析,温度达到最大值时,表示_____。随后溶液温度降低的原因是_____。
(2)实验数据分析可知测得的实际值低于理论值,请写出一点导致这种差异出现的原因_____。