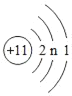
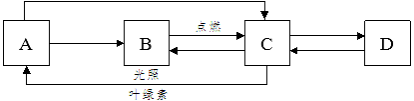
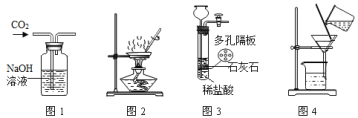
【题目】(1)如表是某种常见金属的部分性质:
颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
将该金属投入稀盐酸中,可产生大量的无色气体。回答以下问题:
①试推断该金属可能的一种用途_____;
②该金属的活动性比铜_____(填“强”或“弱”);
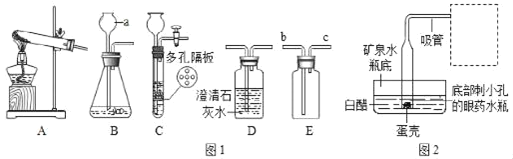
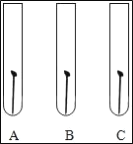
(2)某学生想探究铁生锈是否必须同时有空气和水,他将干净的铁钉放入A、B、C三支干净的试管中,再各加入某些物质或用品进行研究。
①在如图的每支试管中画出并标明所加的物质或用品。
②一周后,编号为_____的试管中铁钉最易生锈。
③写出一氧化碳在高温条件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式:_____。
④铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,其原因是_____。
⑤某炼铁日产含碳3%的生铁310t,问该厂每天至少需要含氧化铁80%的赤铁矿石_____吨。
【题目】某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把40g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下:
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸质量/g | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 3.0 | 2.0 | 1.2 | m |
则求:⑴在第____次反应稀盐酸开始出现剩余,反应停止进行;上表格表m= ______g;
⑵求该石灰石样品中碳酸钙的质量分数为_______;
⑶实验室现要制取二氧化碳气体9.24克,需要上述这种纯度的石灰石质量为_____________?(要求有计算过程)
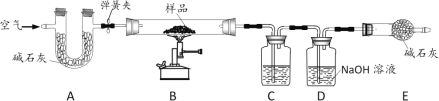
【题目】空气是一种宝贵资源,如利用空气中分离出的氮气合成氨气,合成氨对社会发展和 人类进步做出了巨大贡献,下列是合成氨的工艺流程图:
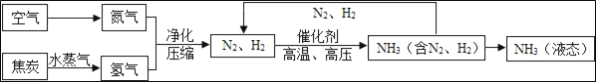
(1)合成氨所需的氮气来自空气,分离液态空气可以得到氮气。
制取氢气的反应过程为:①C+H2O![]() CO+H2②CO+H2O
CO+H2②CO+H2O![]() CO2+H2
CO2+H2
上述反应①中表现还原性的物质是_____(填化学式);反应②中有 CO2生成,它的用途 是_____。(写一种即可)
(2)根据上述流程写出 N2与 H2反应生成NH3的化学方程式_____。
(3)将沸点不同的气体分离开来,常采用液化分离法。如,控制温度在﹣183℃时,可将空气中N2与O2分离,这一过程是_____变化(填“物理”或“化学”)。根据下表中物质的沸点判断,要将产物 NH3与 N2、H2分离开来,温度应该控制在_____℃以下。
物质 | H2 | N2 | O2 | NH3 |
沸点 | ﹣252℃ | ﹣195.8℃ | ﹣183℃ | ﹣33.35℃ |
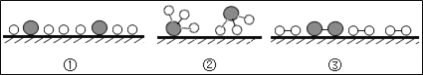
(4)用“![]() ”分别表示 N2、H2、NH3,观察下列微观图,选出符合合成氨化学反应过程的微观顺序图(将下面三张图用序号排列)_____。
”分别表示 N2、H2、NH3,观察下列微观图,选出符合合成氨化学反应过程的微观顺序图(将下面三张图用序号排列)_____。