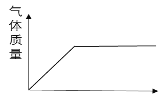
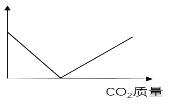
【题目】初二中化学兴趣小组利用如下图装置进行多角度探究常见的气体的制取与性质。
探究一 气体的制取探究
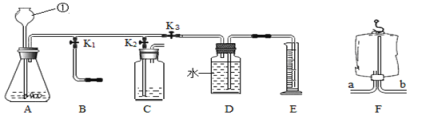
(1)写出仪器名称:①____
(2)用装置A制取二氧化碳反应的化学方程式为:___;若用该装置制取氧气,其化学方程式为:____。
(3)生活中有很多物品可以代替实验仪器。关闭K2和K3,打开K1,若用装置F所示的医用塑料袋排空气法收集CO2,则装置____(“a”或“b”)端与B装置相连。
探究二气体的性质探究
打开K2,关闭K1、K3,用于检验二氧化碳的性质
(4)若装置C中装有紫色石蕊试剂,可观察到___现象,证明了二氧化碳与水发生了反应。若装置C装有澄清石灰水,则反应化学方程式为:___。
探究三生成气体的速率研究
打开K3,关闭K1、K2,可测一段时间内生成气体的速率
(5)实验室用一定质量大理石与稀盐酸反应,所得数据如表(酸足量):
大理石质量(反应前) | 剩余固体质量(反应后) | E装置收集液体体积 | 反应时间 |
12.0g | 2.0g | 2000mL | 100s |
若生成气体的反应速率公式V=△V/△t表示,(△V表示生成气体的体积,△t表示反应时间,CO2的密度约为2g/L),则生成气体的的速率为___mL/s.
(实验思考) 若用该组合装置收集氧气,装置D上方原有的空气对收集气体的体积的测定是否有影响?并说明理由。____。
【题目】根据下列装置,结合所学化学知识回答下列问题:

(1)写出图1中标号仪器的名称:①___。
(2)实验室用高锰酸钾制取氧气时,发生装置应选用___(填字母);其反应的化学方程式为___。如果改用氯酸钾和二氧化锰制取氧气,反应前后固体中二氧化锰的质量分数___(填“增大”、“减小”或“不变”)。
(3)实验室制取少量二氧化碳时,发生装置最好选用___(填字母,下同),收集装置选用___,常用此收集方法的原因是___,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因___
(4)CO2能与NaOH发生反应。
[实验过程]检查装置气密性,如图2所示连接好装置,进行实验。
序号 | 操作步骤 | 实验现象 |
Ⅰ | 打开弹簧夹K1,关闭弹簧夹K2、K3、K4.将20mL水注入锥形瓶I中,关闭弹簧夹K1,振荡瓶J,打开弹簧夹K2. | 无明显现象 |
Ⅱ | 关闭弹簧夹K2,打开弹簧夹K4,将20mL 稀NaOH溶液注入锥形瓶K中,关闭弹簧夹K4,振荡瓶J,打开弹簧夹K3. | 锥形瓶J中的热水剧烈沸腾 |
[实验分析]锥形瓶J的热水剧烈沸腾的原因是___。
[实验反思]有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应。你对该观点的看法是___(选填“赞同”或“不赞同”),理由是___。
【题目】实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究。
Ⅰ.固体的成分分析
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液的pH=7。
③碱石灰是CaO和NaOH的混合物
【提出猜想】猜想Ⅰ:固体未变质,只有NaOH
猜想Ⅱ:固体全部变质,只有Na2CO3
猜想Ⅲ:固体部分变质,是NaOH 和Na2CO3 的混合物
【原因分析】氢氧化钠在空气中变质的原因是_______________(用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是________________,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
同学 | 小钱 | 小徐 | 小陆 |
实验操作 | 加入适量氢氧化钙溶液 | 加入过量氯化钙溶液 | 逐滴加入稀盐酸至过量 |
【实验结论】小钱、小徐的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都得出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小钱的实验操作和现象无法确定猜想Ⅲ正确,理由是__________________。
(二)根据小徐的结论推测小陆实验现象是_________________________________。
Ⅱ 固体中各成分含量
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【进行实验】化学小组同学设计了如下实验装置。
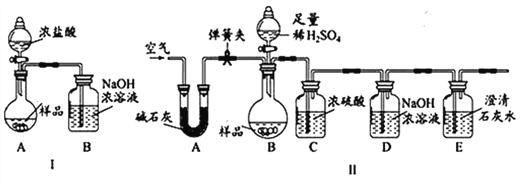
(一)小陆同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是 _______________________;
(二)小钱同学在大家讨论的基础上,设计了装置II。请分析:装置II中A的作用_____________;若无装置C,对测定结果造成的影响是_____________(填“偏大”、“偏小”或“无影响”);E装置的作用是_______________________________。
【实验结论】称取10g样品于圆底烧瓶中,实验结束后,测得装置D增重2.2g,请你计算出样品中Na2CO3质量分数为____________。(写出计算过程)
【反思评价】(一)实验室中的氢氧化钠应密封保存,除了因为空气中有二氧化碳,还因为___________。
(二)若将上述5g氢氧化钠固体全部溶解在45g水中,得到的溶液中氢氧化钠质量分数______10%(填“大于”、“小于”或“等于”)。