测定人体内体液的pH,可以帮助人们了解身体的健康状况,一些体液的近似pH如下:下列液体中,碱性最强的是( )
液体 | 胃液 | 胰液 | 胆汁 | 血浆 |
PH | 0.9﹣1.5 | 7.5﹣8.0 | 7.1﹣7.3 | 7.35﹣7.45 |
A. 胃液 B. 胰液 C. 胆汁 D. 血浆
对比分析不同物质的共性与差异是学习化学的有效方法。下列关于CO2和CO的各项对比,有错误的是( )
选项 | 共性 | 差异性 |
A | 均由分子构成 | 分子的种类不同 |
B | 均由碳元素和氧元素组成 | 元素的质量比不同 |
C | 均能与水化合 | 化合时现象不同 |
D | 常温下均是无色气体 | 相同条件下气体的密度不同 |
A. A B. B C. C D. D
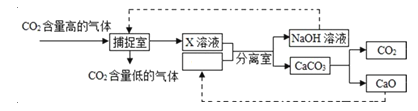
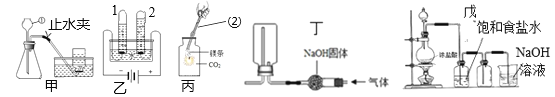
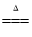 Cl2↑+MnCl2+2HO2制取的,查阅资料得知:氯气有毒、能和碱反应并有剧烈的刺激性,它在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大,则戊装置中饱和食盐水的作用是____。
Cl2↑+MnCl2+2HO2制取的,查阅资料得知:氯气有毒、能和碱反应并有剧烈的刺激性,它在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大,则戊装置中饱和食盐水的作用是____。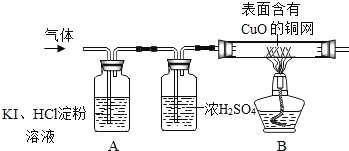
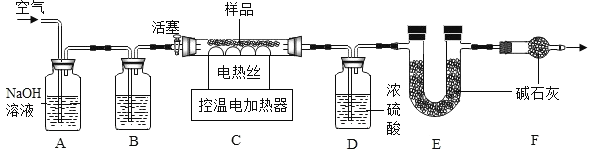
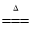 CuO+H2O;CuCO3在200℃~220℃完全分【解析】
CuO+H2O;CuCO3在200℃~220℃完全分【解析】