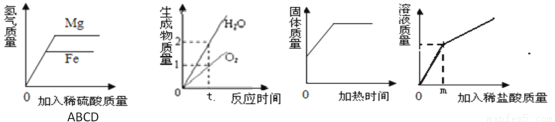
下列有关物质的鉴别、检验、除杂所用试剂或方法正确的是
选项 | 实验目的 | 所用试剂或方法 |
A | 除去铜粉中的碳粉 | 在空气中灼烧 |
B | 除去CO2中少量的CO | 点燃 |
C | 除去氮气中的氧气 | 通过灼热的铜网 |
D | 检验集气瓶中CO2是否收集满 | 将燃着的木条放在集气瓶口 |
A. A B. B C. C D. D
钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是(填字母)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的。
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿(主要成分氧化铁)为原料,在高温下炼铁的化学方程式:;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物。
通过查阅资料知道:
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,化学反应方程式为
H2C2O4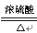 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO2=Na2CO3+H2O
③常温下,Ca(OH)2微溶于水;浓硫酸具有强烈的吸水性
于是他设计了下图的实验装置,结合装置回答下列问题:
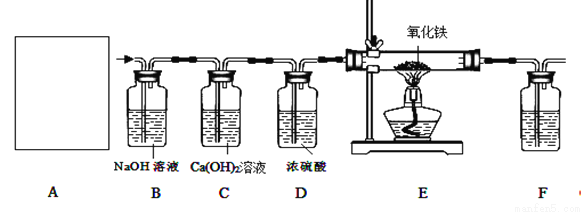
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的(填装置编号);
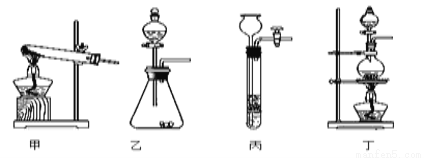
(2)图中装置C的作用是;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的(填试剂名称),反应的化学方程式为;
(4)该装置设计有一个明显缺陷,你认为是。
(5)实验时准确称取一定质量纯净的Fe2O3固体按上图进行实验,当E中固体全部变黑后,继续通入CO直到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a.铁的氧化物在足量的稀盐酸中均能全部溶解。
b.Fe2O3与CO反应的固体生成物可能情况如下:
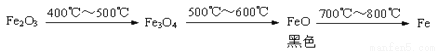
根据“无气泡”猜想,黑色粉末可能是:①Fe3O4;②③。
(6)定量分析用电子天平称量得部分数据如下:
玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
反应前 | 28.20g | 33.00g | 300.0g |
反应后 | 32.84g | 300.4g |
根据上述数据,纯净的Fe2O3固体质量为g,
请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程)(3分)
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式