化学在日常生活中有广泛应用
(1)根据如图衣服标签的部分说明回答下列问题:

①面料中的棉属于_______(填“天然”或“合成”,下同)有机高分子材料,面料中的涤纶属于________有机高分子材料,
②你知道聚酯纤维有下列哪三个优点____________(填序号)
A. 强度高、弹性好 B. 耐磨
C. 吸水性、透气性好 D. 耐化学腐蚀
(2)均衡的膳食结构可以保障身体健康。某种食品的配料标签如图所示:
该配料中富含蛋白质的物质是____________。从营养均衡的角度看,该食品中除水外,还缺少的营养素是____________。
(3)以下是我们日常生活中常用的清洗剂,其名称及有效成分如下表:
生活中的 用品 |
|
活氧彩漂 |
污渍爆炸盐 |
有效成分 | 盐酸 | 过氧化氢 | 过碳酸钠 |
①清除以下物质,可以使用洁厕灵的是____________(填字母序号)。
A. 铁锈 B. 水垢(主要成分为碳酸钙和氢氧化镁) C. 油渍
②“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是____________(填序号)。
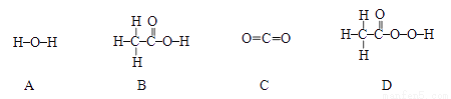
目前,全世界的镍(Ni)消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍常用于各种高光泽装饰漆和塑料生产,也常用作催化剂。
I、制备草酸镍(NiC2O4,其中Ni为+2价):
工业上用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍。
(资料卡片1):
(1).过氧化氢(H2O2)俗称双氧水,是一种液体,受热易分解,可用于实验室制取氧气;过氧化氢能将+2价铁氧化为+3价铁。
(2).金属镍的化学性质类似于铁,与盐酸反应能生成氯化镍(NiCl2)。
根据下列工艺流程图回答问题:
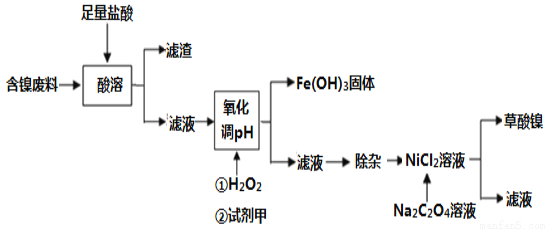
(1)酸溶之后的滤渣中含有的金属是____________(填化学式)。
(2)写出酸溶过程中Ni与盐酸反应的化学方程式____________。
(3)加H2O2时,温度不能太高,其原因是______________________,若H2O2在一开始酸溶时便与盐酸一起加入,则与原步骤酸溶过滤后的滤液相比,该滤液中会增加的金属离子是Cu2+和____________(写离子符号)。
(4)已知Na2C2O4溶液加入NiCl2溶液发生复分解反应,写出该反应的化学方程式_________。
II、镍粉制备:
工业用电解镍液(主要含NiSO4)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉,过程如下:
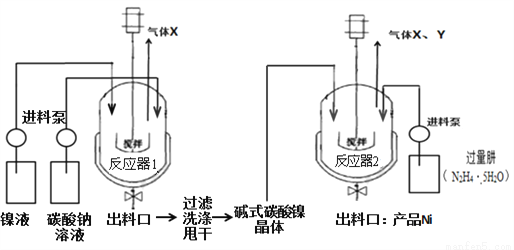
(5)反应器1中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2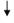 +3Na2SO4+2X,X的化学式为_______________。
+3Na2SO4+2X,X的化学式为_______________。
(6)反应器1的出料口获得的固体洗涤时,需用纯水洗涤,可以用来检验固体洗涤干净的试剂是_______________。
(7)反应器2中产生的气体Y是空气中含量最多的气体,该气体是________(填化学式)。
III、测定碱式碳酸镍晶体的组成:
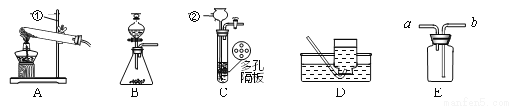
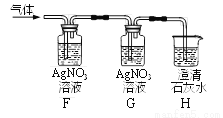
测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成的实验方案及装置如下图:
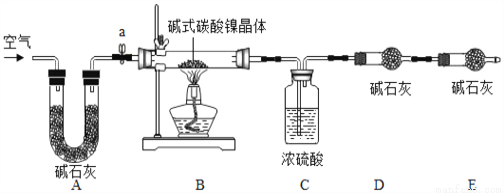
(资料卡片2):
碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O
(实验步骤):
①检查装置气密性;②准确称取3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,分别称量装置C、D、E的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓鼓入一段时间空气;⑥分别准确称量装置C、D、E的质量;⑦根据数据进行计算(相关数据如下表)。
装置C/g | 装置D/g | 装置E/g | |
加热前 | 200.00 | 180.00 | 180.00 |
加热后 | 201.08 | 180.44 | 180.00 |
(实验分析及数据处理):
(8)计算3.77g碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)中镍元素的质量_____g。(写出计算过程,精确到小数点后两位)
Cu Ni+2HCl=NiCl2+H2↑ 防止过氧化氢受热分解 Fe3+ Na2C2O4+ NiCl2=NiC2O4↓+ 2NaCl。 CO2 BaCl2 N2 1.77g 3.77g-1.08g-0.44g=2.25g (2.25g×59/75)×100%=1.77g 【解析】本题通过关于金属镍的探究,考查了金属活动顺序表的应用,复分解反应的应用,质量守恒定律的应用,硫酸根离子的检验,获得...
 TiCl4+2CO
TiCl4+2CO 洁厕灵
洁厕灵