小明在做“盐酸中和氢氧化钠”的实验时,实验前忘记向氢氧化钠溶液中滴加酚酞溶液,导致无法判断中和反应进行的程度,于是小明对反应后溶液的酸碱性进行了探究。
【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液①呈碱性,②呈_____________,③呈______________。
【实验验证】
实验操作 | 实验现象 | 结论与解释 |
| 无色酚酞溶液液呈_______色; | 溶液呈碱性,是因为溶液中含有大量____________(填微粒符号) |
无色酚酞溶液不变色 | 溶液呈__________; |
【继续验证】
实验操作 | 实验现象 | 结论与解释 |
| 粉末部分或全部消失,溶液变为黄色; | 溶液呈_____性,反应的化学方程式是___________ |
________________________; | 溶液呈_______; |
利用表中装置进行下列实验。
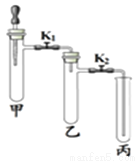
实验装置 | 实验1 | 实验2 |
| ①甲试管中放入少量MnO2,滴管中放入过氧化氢溶液,乙、丙中分别放入一小块白磷依次加入适量80℃的水,白磷均不燃烧 ②打开K1、K2,将过氧化氢溶液滴入试管,观察到乙试管中白磷不燃烧,丙中白磷燃烧 ③一段时间后,丙中导管内液 面上升 | ①关闭K1,打开K2,甲试管中充满CO2,滴管中放入浓NaOH溶液;乙试管中放入适量铁粉,丙中放入约半试管稀盐酸 ②将浓NaOH溶液滴入甲试管中,一段时间后,打开K1 ③一段时间后,观察乙、丙试管中的现象 |
(1)实验1:甲中发生反应的化学方程式是_______________,对比乙和丙中的实验现象,本实验欲探究的燃烧条件是_____________;步骤③中“丙中导管内液面上升”的原因是________________。
(2)实验2:甲中发生反应的化学方程式为____________;步骤③乙中的现象是_____________;丙试管中的现象是_________。
2H2O22H2O+O2↑ 可燃物燃烧需要与氧气接触 甲中反应放热,一段时间后温度降低,导致压强减小 CO2+2NaOH==Na2CO3+H2O 丙试管中稀盐酸被倒吸入乙试管,产生大量气泡,溶液由无色变为浅绿色 开始丙试管中稀盐酸被倒吸入,稍后有气泡产生 【解析】本题主要考查碱、酸的性质,燃烧条件的探究。解答时要根据各种物质的性质,气体压强的知识,结合各方面条件进行分析、判断,从而得出正确的...制取干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应,设计如下探究实验。


【查阅资料】
(1)碳酸钠、水、二氧化碳可以化合生成碳酸氢钠。
(2)20℃,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示
物质 | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 110 | 21.8 | 9.6 |
经测定,实验过程中装置D的温度保持20℃。
【定性探究】
(1)仪器a的名称是____________________;
(2)装置B中盛有 NaHCO3溶液,目的是吸收装置A中挥发出的HCl气体,写出B中发生反应的化学方程式:___________;
(3)装置C的作用是________,选择________(选填E、F)达到实验目的;
(4)在实验过程中装置D中观察到__________,说明CO2和NaOH溶液能发生反应。
【定量计算】
(5)装置D中盛有的210g20℃NaOH饱和溶液中含有NaOH___________g;
(6)装置D中NaOH全部转化成Na2CO3时,理论上最多可以生成Na2CO3_______________克?
(7)当向装置D中通入足量的CO2时,可以将NaOH全部转化为NaHCO3,实验过程中会析出的 NaHCO3质量________g(不考虑结晶水)。
长颈漏斗 NaHCO3+HCl==NaCl+H2O+CO2↑ 吸收二氧化碳中混有的水蒸气 E 有固体析出 110 145.75g 221.4g 【解析】本题考查了气体的净化和干燥,溶解度的应用和计算,化学方程式的计算等。 (1)仪器a的名称是长颈漏斗; (2)装置B中盛有 NaHCO3溶液,目的是吸收装置A中挥发出的HCl气体,NaHCO3和HCl反应生成氯化钠、水和二氧化碳,反...