1.相同质量的钠、镁、铝所含原子数目的相对多少正确的是( )
| A. | 钠最少 | B. | 钠最多 | C. | 铝最多 | D. | 镁最少 |
20.只用下列鉴别方法不能把待鉴别的物质区分开的是( )
| 待鉴别的物质 | 鉴别方法 | |
| A | 二氧化碳和氮气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
| B | 硬水和软水 | 加肥皂水,振荡,观察产生泡沫情况 |
| C | 过氧化氢溶液和水 | 加二氧化锰,观察有无气泡产生 |
| D | 氧气和空气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
| A. | A | B. | B | C. | C | D. | D |
19.某同学观察演示实验后,描述的实验现象正确的是( )
| A. | 红磷在空气中燃烧产生大量的烟雾 | |
| B. | 氢气在空气中燃烧有淡蓝色火焰 | |
| C. | 硫在空气中燃烧产生有刺激性气味的二氧化硫气体 | |
| D. | 木炭空气中剧烈燃烧,发出黄色火焰,有能使澄清石灰水变浑浊的气体生成 |
18.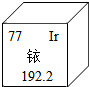 南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
 南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )| A. | 铱的原子序数为115 | B. | 铱原子的核电荷数为77 | ||
| C. | 铱的相对原子质量为192.2g | D. | 铱原子的核内中子数为80 |
17.下列元素属于金属元素的是( )
| A. | 氦 | B. | 硫 | C. | 钙 | D. | 溴 |
16. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的符号表达式(或化学方程式)2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释O2比N2化学性质活泼.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的符号表达式(或化学方程式)2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.证明猜想正确 |
12.如图是元素周期表的一部分,请回答相关问题:

(1)氟元素与氯元素位于同一纵行的原因是最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子,镁元素与氯元素形成化合物的化学式是MgCl2.
(2)M2-与Ne 核外电子排布相同,则M 元素的名称为氧.
(3)物质之间既相互联系,又存在规律,这是我们学好化学应该掌握的一种基本方法.请
你仿照下表中的示例,找出H2,CH4、H2S、NH3 四种气体之间存在的规律,并排列出顺序,将答案填在下表中的空格内.
0 167855 167863 167869 167873 167879 167881 167885 167891 167893 167899 167905 167909 167911 167915 167921 167923 167929 167933 167935 167939 167941 167945 167947 167949 167950 167951 167953 167954 167955 167957 167959 167963 167965 167969 167971 167975 167981 167983 167989 167993 167995 167999 168005 168011 168013 168019 168023 168025 168031 168035 168041 168049 211419

(1)氟元素与氯元素位于同一纵行的原因是最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子,镁元素与氯元素形成化合物的化学式是MgCl2.
(2)M2-与Ne 核外电子排布相同,则M 元素的名称为氧.
(3)物质之间既相互联系,又存在规律,这是我们学好化学应该掌握的一种基本方法.请
你仿照下表中的示例,找出H2,CH4、H2S、NH3 四种气体之间存在的规律,并排列出顺序,将答案填在下表中的空格内.
| 规律 | 排序 |
| 示例:标准状况下,密度由小到大 | H2、CH4、NH3、H2S |
| 一个分子中所含原子总数由小到大 | H2、H2S、NH3、CH4 |
| 相对分子质量由小到大 | H2、CH4、NH3、H2S |
| 所含氢元素的质量分数由小到大 | H2S、NH3、CH4、H2 |


 ;
;