17.在密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:下列说法正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 20 | 5 |
| 反应后质量/g | 待测 | 10 | 8 | 13 |
| A. | 反应后X的质量为6g | B. | 该反应的反应物是X、Y | ||
| C. | 参加反应的X、Z的质量比是1:3 | D. | 该反应可能是化合反应 |
16.下列化学方程式中符合题意,且书写正确的是( )
| A. | 氧化铁在加热时被一氧化碳还原成铁:Fe2O3+CO$\frac{\underline{\;\;△\;\;}}{\;}$ 2Fe+2CO2 | |
| B. | 甲烷的完全燃烧:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | |
| C. | 实验室制备氢气:Mg+H2SO4═MgSO4+H2↑ | |
| D. | 碳酸氢钠与稀硫酸反应:NaCO3+H2SO4═NaSO4+H2O+CO2↑ |
15.下列除去杂质(括号内为杂质)选用的试剂正确的是( )
| A. | O2(水蒸气)-浓硫酸 | B. | CaO(CaCO3)-稀盐酸 | ||
| C. | Cu(CuO)-蒸馏水 | D. | NaOH(Na2SO4)-BaCl2溶液 |
14.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某化学实验小组对组成中含Fe元素或Cu元素的红色粉末进行了一系列的实验.请回答实验中有关问题:
实验一:探究红色粉末的成分
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和Cu2+,在空气中加热生成CuO.②Cu能与溶液中的Fe3+作用生成Cu2+和Fe2+.③溶液中的Fe3+遇到KSCN溶液呈红色.④H2O2在酸性条件下能将Fe2+转化为Fe3+
[提出假设]假设1:红色粉末是Fe2O3假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物.
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN溶液.
(1)若假设1成立,则实验现象是固体完全溶解,溶液变为血红色.
(2)若假设2成立,则实验现象是溶液变为蓝色,最终溶液中仍有红色固体.
(3)若固体粉末完全溶解,滴加KSCN溶液时溶液不变红色,则红色粉末中一定有Fe2O3和Cu2O此时发生反应的一个复分解反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
[实验结果]经实验分析,假设3是正确的.
实验二:测定Cu2O的质量分数
(4)取a g该固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
实验三:利用该红色粉末制取较纯净的胆矾经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下表:
实验室可供选择试剂有:A.氨水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
该实验小组设计实验方案如下:

(5)请回答:
①试剂1为B(从可供选择试剂中选择并填出对应字母编号,②同);
②试剂2为D;
③固体X的化学式为Fe(OH)3;
④操作I为加热浓缩,冷却结晶.
0 166755 166763 166769 166773 166779 166781 166785 166791 166793 166799 166805 166809 166811 166815 166821 166823 166829 166833 166835 166839 166841 166845 166847 166849 166850 166851 166853 166854 166855 166857 166859 166863 166865 166869 166871 166875 166881 166883 166889 166893 166895 166899 166905 166911 166913 166919 166923 166925 166931 166935 166941 166949 211419
实验一:探究红色粉末的成分
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和Cu2+,在空气中加热生成CuO.②Cu能与溶液中的Fe3+作用生成Cu2+和Fe2+.③溶液中的Fe3+遇到KSCN溶液呈红色.④H2O2在酸性条件下能将Fe2+转化为Fe3+
[提出假设]假设1:红色粉末是Fe2O3假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物.
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN溶液.
(1)若假设1成立,则实验现象是固体完全溶解,溶液变为血红色.
(2)若假设2成立,则实验现象是溶液变为蓝色,最终溶液中仍有红色固体.
(3)若固体粉末完全溶解,滴加KSCN溶液时溶液不变红色,则红色粉末中一定有Fe2O3和Cu2O此时发生反应的一个复分解反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
[实验结果]经实验分析,假设3是正确的.
实验二:测定Cu2O的质量分数
(4)取a g该固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
实验三:利用该红色粉末制取较纯净的胆矾经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
该实验小组设计实验方案如下:

(5)请回答:
①试剂1为B(从可供选择试剂中选择并填出对应字母编号,②同);
②试剂2为D;
③固体X的化学式为Fe(OH)3;
④操作I为加热浓缩,冷却结晶.
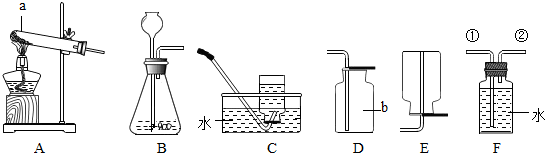

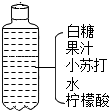 根据图中自制汽水的配料回答问题.
根据图中自制汽水的配料回答问题.