16. 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)
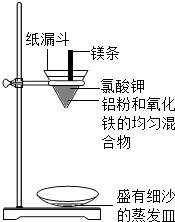
实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应.
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
12.下列关于化学实验的“目的一操作一现象一结论”的描述正确的是( )
0 165533 165541 165547 165551 165557 165559 165563 165569 165571 165577 165583 165587 165589 165593 165599 165601 165607 165611 165613 165617 165619 165623 165625 165627 165628 165629 165631 165632 165633 165635 165637 165641 165643 165647 165649 165653 165659 165661 165667 165671 165673 165677 165683 165689 165691 165697 165701 165703 165709 165713 165719 165727 211419
| A. | 检验某混合气体中是否含有CO2气体 通入澄清石灰水中 无明显现象 该气体中不含CO2 | |
| B. | 除去KCl中的少量K2CO3 稀盐酸 有气泡产生 K2CO3已被除完 | |
| C. | 区分硬水和蒸馏水 肥皂水 产生大量泡沫 该液体为蒸馏水 | |
| D. | 用排空气法收集CO2时检验集气瓶中CO2是否集满 将燃烧的木条伸人瓶内 木条熄灭 瓶内CO2已集满 |



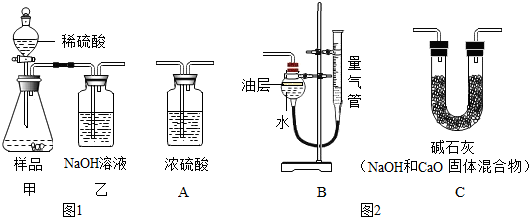
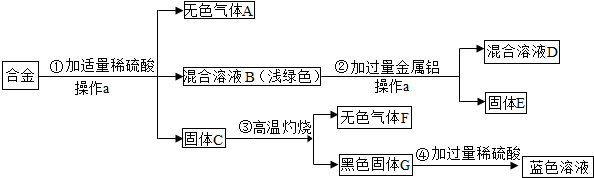
 ,氯原子的最外层电子数为7.下列图中微粒共表示三种元素,其中与氯原子具有相似化学性质的是D(填序号).
,氯原子的最外层电子数为7.下列图中微粒共表示三种元素,其中与氯原子具有相似化学性质的是D(填序号).
 ,则x的数值可能是下列中的CD.
,则x的数值可能是下列中的CD. 小华按图配方自制了一瓶清凉甘甜的汽水.根据图中信息回答:
小华按图配方自制了一瓶清凉甘甜的汽水.根据图中信息回答: